주요 차이 - 흡열 대 발열 반응
화학 반응은 두 그룹으로 나눌 수 있으며, 주변 환경과 반응이 발생하는 시스템 사이의 에너지 전달에 따라 흡열 반응과 발열 반응으로 나눌 수 있습니다. 특정 화학 반응을 흡열 또는 발열로 분류하기 위해 반응물과 제품 사이의 엔탈피 변화를 계산할 수 있습니다. 그렇지 않은 경우 반응 혼합물의 온도 변화를 관찰 할 수 있습니다. 흡열과 발열 반응의 주요 차이점은 흡열 반응이 주변에서 에너지를 흡수하는 반면, 발열 반응은 주변에 에너지를 방출한다는 것입니다.
주요 영역을 다루었습니다
1. 흡열 반응이란 무엇입니까
- 정의, 속성, 예
2. 발열 반응이란 무엇입니까
- 정의, 속성, 예
3. 흡열 및 발열 반응의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :연소, 흡열, 엔탈피, 발열, 열, 내부 에너지
흡열 반응이란 무엇인가
흡열 반응은 주변에서 열 에너지를 흡수하는 화학 반응입니다. 이것은 흡열 반응의 개시 및 진행을 위해 외부에서 에너지를 제공해야한다는 것을 의미합니다. 결과적으로 시스템의 온도는 감소합니다.
시스템이 외부에서 에너지를 흡수함에 따라 엔탈피 변화는 긍정적 인 값을 취합니다. 엔탈피는 시스템의 내부 에너지의 합계와 해당 환경에서 해당 시스템의 부피와 압력을 유지하는 데 필요한 에너지입니다. 처음에, 시스템의 엔탈피는 반응물의 엔탈피의 합과 같다. 흡열 반응의 끝에서, 에너지의 흡수로 인해 엔탈피 또는 제품의 에너지가 더 높다. 이것은 다음과 같이 설명 할 수 있습니다.
a +b → c +d
ΔH ={h c +h d } - {h a +h b }
ΔH =(h 제품 ) - (h 반응물 ) =긍정적 값
여기서,
ΔH 반응 후에 발생하는 엔탈피 변화,
hc 및 hd 제품 C와 D의 엔탈피는 각각 입니다
ha 및 HB 반응물 A와 B의 엔탈피는 각각.
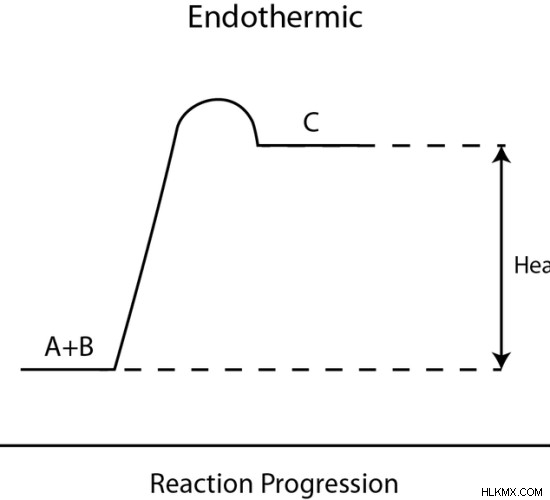
그림 1 :흡열 반응의 엔탈피 및 흡열 반응
흡열 반응은 반응이 일어나는 비이커 또는 테스트 튜브를 만지면 쉽게 인식 할 수 있습니다. 비커는 이전보다 더 차갑게 느낄 것입니다. 이것은 외부에서 에너지를 흡수하기 때문입니다.
흡열 반응의 예
- 물에 염화 암모늄 고체 용해 :
nh 4 cl (s) +h 2 o (l) +열 → nh 4 cl (aq)
- 염화 칼륨과 물을 혼합 :
kcl (s) +h 2 o (l) +열 → kcl (aq)
- 에탄 산 나트륨과 반응하는 탄산나트륨 :
ch 3 cooh (aq) +na 2 Co 3 (s) +열 → ch 3 coona (aq) +h (aq) +Co
"열"은 반응 방정식의 오른쪽에 포함됩니다. 이것은 시스템에 의한 열 흡수를 나타 내기위한 것입니다.
발열 반응이란 무엇인가
발열 반응은 주변에 열 에너지를 방출하는 화학 반응입니다. 이것은 화학 반응이 진행될 때 에너지가 외부로 방출된다는 것을 의미합니다. 내부 에너지가 시스템에서 방출되기 때문에 제품의 엔탈피는 반응물의 엔탈피보다 낮습니다. 이것은 다음과 같이 설명 할 수 있습니다.
p +q → r +s
ΔH ={h r +h s } - {h p +h q }
ΔH =(h 제품 ) - (h 반응물 ) =음수 값
엔탈피의 변화는 이제 반응물의 내부 에너지가 에너지 방출로 인해 덜 부정적인 값입니다. 발열 반응이 진행됨에 따라 시스템의 온도가 증가합니다. 따라서, 반응이 일어나고있는 용기의 벽에 닿아 특정 화학 반응이 흡열인지 발열인지 여부를 추측 할 수있다. 발열 반응에서 용기는 따뜻해집니다.
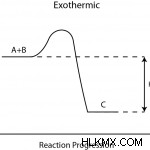
그림 2 :발열 반응의 반응물 및 생성물의 엔탈피
발열 반응의 예
- 수소 가스 연소 :
2H 2 (g) +o 2 (g) → 2h 2 o (l) +열
- 에탄올 연소 (완전 연소) :
ch 3 ch 2 오 (l) +3o 2 (g) → 2co 2 (g) +3H 2 o (l)
흡열과 발열 반응의 차이
정의
흡열 반응 : 흡열 반응은 주변에서 열 에너지를 흡수하는 화학 반응입니다.
발열 반응 : 발열 반응은 주변에 열 에너지를 방출하는 화학 반응입니다.
온도
흡열 반응 : 흡열 반응의 진행에 따라 온도가 감소합니다.
발열 반응 : 발열 반응의 진행에 따라 온도가 증가합니다.
엔탈피
흡열 반응 : 반응물의 엔탈피는 흡열 반응에서 제품의 엔탈피보다 낮습니다.
발열 반응 : 반응물의 엔탈피는 발열 반응에서 생성물보다 높다.
엔탈피 변화
흡열 반응 : 엔탈피 (ΔH)의 변화는 흡열 반응에 대한 양의 값입니다.
발열 반응 : 엔탈피 (ΔH)의 변화는 발열 반응에 대한 부정적인 값입니다.
에너지
흡열 반응 : 흡열 반응에서 시스템에 에너지가 제공되어야합니다.
발열 반응 : 흡열 반응에서 시스템에서 에너지가 방출됩니다.
결론
화학 반응은 시스템과 주변의 에너지 전달에 따라 흡열 및 발열 반응으로 분류됩니다. 흡열 성 반응과 발열 반응의 주요 차이점은 흡열 반응이 주변에서 에너지를 흡수하는 반면, 발열 반응은 주변 . 에 에너지를 방출한다는 것입니다. 각각의 모든 화학 반응은 반응의 엔탈피 변화를 계산 하여이 두 범주로 분류 할 수 있습니다.