주요 차이 - 내부 대 외부 궤도 복합체
조정 복합체는 상이한 원자 또는 원자 그룹으로 둘러싸인 중앙 원자 또는 이온으로 구성된 분자 구조이다. 중앙 원자는 종종 전이 금속 원자입니다. 주변 원자 또는 그룹을 리간드라고합니다. 이들 리간드는 좌표 공유 결합을 통해 중앙 원자에 결합된다. 이들 결합은 리간드의 S와 P 분자 궤도와 금속 원자의 D 원자 궤도 사이에 형성된다. 원자가 결합 이론에 따르면, 금속 원자의 원자 궤도는 결합을 형성하기 전에 혼성화를 겪는다. 이 혼성화 패턴에 기초한 두 가지 유형의 배위 복합체는 내부 궤도 복합체와 외부 궤도 복합체가있다. 이 이름은 금속 원자의 S 및 P 궤도의 위치와 관련하여 D 궤도의 위치에 따라 제공됩니다. 내부와 외부 궤도 복합체의 주요 차이점은 내부 궤도 복합체의 중앙 금속 원자의 원자 궤도의 혼성화는 내부 쉘 d 궤도를 포함하는 반면, 외부 orbital complex의 중앙 금속 원자의 원자 궤도의 하이브리드 화는 가장 껍질 d 궤도를 포함한다는 것입니다.
주요 영역을 다루었습니다
1. 내부 궤도 복합체는 무엇입니까
- 정의, 구조의 설명
2. 외부 궤도 복합체는 무엇입니까
- 정의, 구조의 설명
3. 내부와 외부 궤도 복합체의 차이점은 무엇입니까
- 주요 차이점 비교
핵심 용어 :공유 결합, 배위 복합체, 하이브리드 화, 내부 궤도 복합체, 리간드, 궤도, 외부 궤도 복합체, 전이 금속, 원자가 결합 이론
내부 궤도 복합체
내부 궤도 복합체는 내부 쉘의 d 궤도를 포함하여 원자 궤도의 하이브리드 화 및 외부 쉘의 p 궤도를 포함하는 원자 궤도의 하이브리드 화를 갖는 중앙 금속 원자로 구성된 배위 화합물입니다. 다시 말해, 이들 복합체의 중심 금속 원자는 원자 궤도의 혼성화를 위해 내부 쉘 d 궤도를 사용한다. 따라서, 이러한 d 궤도는 s와 p 궤도보다 에너지 수준이 낮다.
내부 궤도 복합체에서 금속 원자의 가장 일반적인 혼성화는 dsp입니다. 그러나 DSP와 같은 다른 혼성화도있을 수 있습니다. 내부 궤도 복합체의 형성을 이해하기 위해 예제를 고려해 봅시다.
.예
[CO (NH 3 )
코발트 (CO)의 전자 구성은 [ar] 3d4s.
입니다
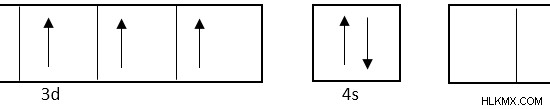
nh 3 이후 리간드에는 전하가 없으며, CO 원자의 산화 상태는 +3이어야합니다.
CO의 전자 구성은 [ar] 3d.
입니다
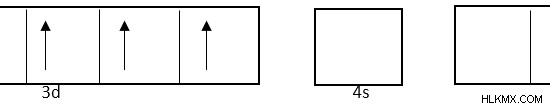
6 리간드와 6 개의 좌표 공유 결합을 형성하기 위해 (NH 3 . ), 6 원자 궤도는 혼성화되어야합니다. 따라서, 3D 궤도 중 2 개는 1 개의 4S 궤도 및 3 개의 4p 궤도로 혼성화됩니다. 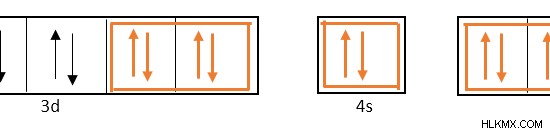
하이브리드 화에 관여하는 d 궤도는 전자 쉘 3에 있고 s 및 p 궤도는 전자 쉘 4에 있기 때문에,이 금속 원자로 형성된 배위 복합체를 내부 궤도 복합체라고합니다. 오렌지색의 화살표는 6 개의 리간드에 의해 기증 된 6 개의 고독한 전자 쌍을 보여줍니다.
외부 궤도 복합체는 무엇입니까
외부 궤도 복합체는 가장 바깥 쪽 쉘에서 S, P 및 D 궤도를 포함하는 원자 궤도의 하이브리드 화를 갖는 중앙 금속 원자로 구성된 배위 화합물입니다. 여기서, 혼성화에 관여하는 모든 원자 궤도는 동일한 에너지 수준에있다. 이 하이브리드 화에 관여하는 D 궤도는 S 및 P 궤도 외부에 있기 때문에, 이들 금속 원자로부터 형성된 복합체를 외부 궤도 복합체라고한다.
.이 유형의 복합체에서 관찰 할 수있는 가장 일반적인 하이브리드 화는 SPD입니다. 이것은 아래와 같이 예제를 사용하여 설명 할 수 있습니다.
예
[cof 6 ] 복잡한 조정 단지입니다.
코발트 (CO)의 전자 구성은 [ar] 3d4s.
입니다하나의 F 원자의 전하는 -1입니다. 따라서 CO 원자의 산화 상태는 복합체의 전체 전하를 균형있게하기 위해 +3이어야합니다.
CO의 전자 구성은 [ar] 3d.
입니다
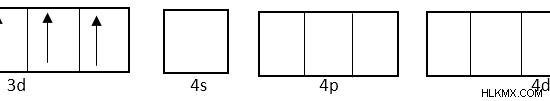
좌표 공유 결합을 형성하기 위해 4S 궤도, 3 개의 4p 궤도 및 4d 궤도 중 2 개는 혼성화됩니다. 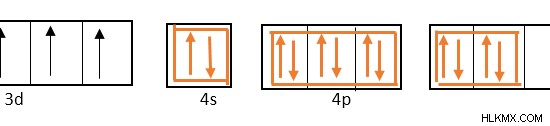
4S, 4P 및 4D 궤도는 혼성화에 관여하기 때문에 불소 이온에서 오는 고독한 전자 쌍은 이들 하이브리드 궤도에 채워진다. D 궤도는 S 및 P 궤도 외부에 위치하므로, 이들 금속 원자로부터 형성된 복합체를 외부 궤도 복합체라고한다.
.내부와 외부 궤도 복합체의 차이
정의
내부 궤도 복합체 : 내부 궤도 복합체는 내부 D 궤도를 포함하여 원자 궤도의 하이브리드 화를 겪는 중심 금속 원자를 갖는 좌표 화합물이다.
외부 궤도 복합체 : 외부 궤도 복합체는 가장 바깥 쪽 D 궤도를 포함하여 원자 궤도의 하이브리드 화를 겪는 중심 금속 원자를 갖는 좌표 화합물이다.
가장 일반적인 혼성화
내부 궤도 복합체 : 내부 궤도 복합체에서 금속 원자의 가장 흔한 혼성화는 DSP입니다.
외부 궤도 복합체 : 외부 궤도 복합체에서 금속 원자의 가장 일반적인 하이브리드 화는 sp d.
입니다.에너지 수준
내부 궤도 복합체 : 내부 궤도 복합체에서, 하이브리드 화에 관여하는 D 궤도는 S 및 P 궤도보다 낮은 에너지 수준에있다.
외부 궤도 복합체 : 외부 궤도 복합체에서, 하이브리드 화에 관여하는 d 궤도는 s 및 p 궤도와 동일한 에너지 수준에있다.
전자 쉘
내부 궤도 복합체 : 내부 궤도 복합체는 중앙 금속 원자에서 하이브리드 화를 위해 내부 쉘 D 궤도를 사용하는 금속 원자로 구성됩니다.
외부 궤도 복합체 : 외부 궤도 복합체는 중앙 금속 원자에서 하이브리드 화를 위해 가장 바깥 쪽 쉘 D 궤도를 사용하는 금속 원자로 구성됩니다.
결론
원자 궤도의 하이브리드 화는 원자 궤도의 중첩을 통해 두 원자 사이의 결합을 설명하기 위해 원자가 결합 이론에서 사용되는 개념입니다. 이 이론은 조정 복합체의 결합을 설명하는 데 사용될 수 있습니다. 여기서, 중심 원자의 혼성화에 사용 된 d 궤도의 에너지 수준에 따르면, 배위 복합체는 내부 궤도 복합체 및 외부 궤도 복합체로서 두 가지 유형으로된다. 내부와 외부 궤도 복합체의 주요 차이점은 내부 궤도 복합체의 중앙 금속 원자의 원자 궤도의 혼성화는 내부 쉘 d 궤도를 포함하는 반면, 외부 orbital 복합체의 중앙 금속 원자의 원자 궤도의 하이브리드 화는 가장 바깥 쪽 쉘 d 궤도를 포함한다는 것입니다.
.






