주요 차이 - 활성화 된 복합체 대 전이 상태
화학 반응은 물리적 형태 또는 핵 반응의 변화와 구별되는 물질의 분자 또는 이온 구조를 재 배열하는 과정입니다. 화학 반응은 단일 단계를 통해 직접 발생하거나 여러 단계를 통해 발생할 수 있습니다. 활성화 된 복합체 및 전이 상태는 여러 단계 또는 단계를 가진 화학 반응에 관한 두 가지 용어입니다. 활성화 된 복합체는 화학 반응의 진행 동안 형성된 중간 분자의 수집을 의미한다. 여기서, 화학 반응의 진행은 반응물을 생성물로 전환시키는 것을 지칭한다. 화학 반응의 전이 상태는 가장 높은 잠재적 에너지와 중간체입니다. 활성화 된 복합체와 전이 상태의 주요 차이점은 활성화 된 복합체가 가능한 모든 중간체를 나타내는 반면 전이 상태는 가장 높은 잠재적 에너지를 가진 중간체를 지칭한다는 것입니다.
주요 영역을 다루었습니다
1. 활성화 된 것
- 정의, 설명
2. 전환 상태
- 정의, 설명
3. 활성화 된 복합체와 전이 상태의 관계는 무엇입니까
4. 활성화 된 복합체와 전이 상태의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :활성화 된 복잡한, 화학 반응, 중간, 제품, 잠재적 에너지, 반응물, 전이 상태

활성화 된 단지
활성화 된 복합체는 화학 반응의 진행 동안 형성된 중간 분자의 수집을 나타냅니다. 활성화 된 복합체는 반응물의 원자의 불안정한 배열이다. 따라서, 중간 배열 또는 활성화 된 복합체는 반응물보다 더 높은 잠재적 에너지를 갖는다. 불안정성으로 인해 활성화 된 단지는 매우 짧은 기간 동안 존재합니다.
활성화 된 복합체는 최종 제품을 형성하거나 형성하지 않을 수도 있습니다. 이것은 활성화 된 복합체가 때때로 뒤로 이동하여 반응물을 생성물을 형성하는 것보다 다시 제공한다는 것을 의미합니다. 화학 반응은 화학 결합의 파손 및 형성을 포함합니다. 활성화 된 복합체는 다른 원자 사이에 결합이 파손되고 형성 될 때 형성됩니다.
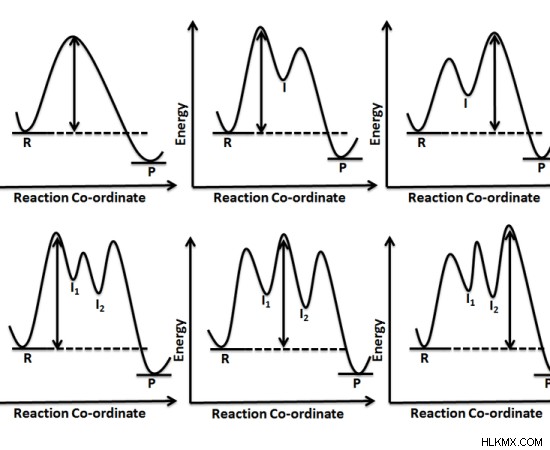
그림 1 :다른 중간체와의 다른 화학 반응
그러나 화학적 결합을 깨고 형성하기 위해서는 에너지가 반응물에 제공되어야합니다. 따라서, 반응물은 반응이 발생하기 위해 적절한 방향으로 서로 콜로이드를한다. 이러한 충돌은 활성화 된 복합체를 형성한다.
전이 상태
전이 상태는 가장 높은 잠재적 에너지를 포함하는 화학 반응의 중간체입니다. 중간체가 하나만있는 화학 반응의 경우, 그 중간체는 전이 상태로 간주됩니다. 2 단계 이상의 화학 반응에는 3 단계가 있습니다. 반응물 만있는 초기 단계, 중간체를 갖는 전이 상태 및 제품과의 최종 단계. 따라서 전이 상태는 반응물이 생성물로 변환되는 단계를 나타냅니다.
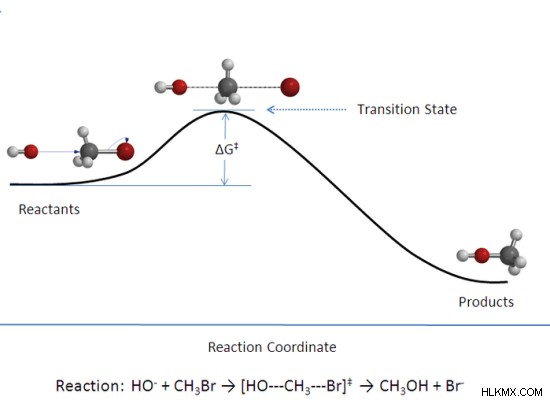
그림 2 :전환 상태
전이 상태가 반응물을 다시 형성하기 위해 다시 떨어지지 않고 제품을 형성 할 확률이 높습니다. 화학 반응을 성공적으로 만들기 위해, 반응물 분자는 적절한 방향으로 서로 콜로이드를해야한다. 전이 상태 또는 가장 높은 잠재적 에너지를 가진 중간체는 매우 불안정합니다. 따라서 오랜 시간 동안 존재하지 않습니다. 이것은 화학 반응의 전이 상태를 포착하기가 어렵다.
활성화 에너지
화학 반응의 활성화 에너지는 반응으로부터 생성물을 얻기 위해 극복 해야하는 에너지 장벽입니다. 반응물이 제품으로 전환하는 데 필요한 최소 에너지입니다. 따라서 활성화 에너지는 화학 반응의 전이 상태의 잠재적 에너지와 같습니다.
활성화 된 복합체와 전이 상태 간의 관계
- 화학 반응에 중간 분자가 하나만 있으면 활성화 된 복합체와 전이 상태가 동일합니다.
활성화 된 복합체와 전이 상태의 차이
정의
활성화 된 단지 : 활성화 된 복합체는 화학 반응의 진행 동안 형성된 중간 분자의 수집을 말한다.
전환 상태 : 전이 상태는 가장 높은 잠재적 에너지를 포함하는 화학 반응의 중간체입니다.
잠재적 에너지
활성화 된 단지 : 활성화 된 복합체는 반응물보다 높은 잠재적 에너지를 갖는다.
전환 상태 : 전환 상태는 다른 중간 구조 중에서 가장 높은 잠재적 에너지를 가지고 있습니다.
제품 형성
활성화 된 단지 : 활성화 된 복합체는 반응의 최종 생성물을 형성 할 수 있거나 생성물을 제공하지 않고 반응물을 역전시킬 수 있습니다.
전환 상태 : 전이 상태는 반응물을 다시 형성하는 대신 생성물을 형성 할 확률이 높다.
결론
일부 화학 반응은 여러 단계를 통해 발생합니다. 세 가지 주요 단계가 있습니다 :반응물이있는 초기 단계, 중간 분자를 갖는 전이 상태 및 제품의 최종 단계. 활성화 된 복합체 및 전이 상태는 이러한 유형의 화학 반응과 관련하여 설명 된 두 가지 용어입니다. 활성화 된 복합체와 전이 상태의 주요 차이점은 활성화 복합체가 가능한 모든 중간체를 나타내는 반면 전이 상태는 가장 높은 잠재적 에너지를 갖는 중간체를 지칭한다는 것입니다.