주요 차이 - 금속 산화물 대 비 금속 산화물
산화물은 하나 이상의 산소 원자를 함유하는 화합물입니다. 금속은 우수한 전기 및 열전도율, 빛의 반사율, 가상 및 연성과 같은 독특한 특성을 가진 물질입니다. 금속은 금속 할로이드, 금속 산화물, 금속 황화물 등과 같은 다양한 화합물을 형성합니다. 비금속은 금속 특성을 나타내지 않는 화학 요소입니다. 주기율표에서 P 블록의 대부분의 멤버는 비금속입니다. 원소의 산화물을 고려할 때 금속 산화물과 비 금속 산화물이 있습니다. 금속 산화물은 금속의 산화물입니다. 비금속 산화물은 비금속의 산화물입니다. 금속 산화물과 비 금속 산화물의 주요 차이점은 금속 산화물이 기본 화합물이고 비금속 산화물은 산성 화합물이라는 것입니다.
주요 영역을 다루었습니다
1. 금속 산화물이란?
- 정의, 속성, 다른 유형
2. 비 금속 산화물이란?
- 정의, 속성, 다른 유형
3. 금속 산화물과 비 금속 산화물의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :산, 염기, 금속, 금속 산화물, 비금속, 비금속 산화물, 산화물, 산화물, 과산화물, 과산화물

금속 산화물이란 무엇입니까
금속 산화물은 금속과 하나 이상의 산소 원자를 함유하는 화학 화합물입니다. 여기서, 산소의 산화 수는 -2이고, 금속이 양이온 인 음이온이다. 알칼리 금속 (그룹 1 요소), 알칼리성 지구 금속 (그룹 2 요소) 및 전이 금속 (일부 D 블록 요소)은 이온 산화물을 형성합니다. 그러나 높은 산화 상태를 나타내는 금속은 공유 특성을 가진 산화물에서 나올 수 있습니다.
금속 산화물은 결정질 고체 화합물입니다. 이들 화합물은 금속 양이온 및 산화 음이온을 함유한다. 이 화합물은 종종 기본 화합물이며 물과 반응하여 염기를 제공 할 수 있습니다. 그렇지 않다면, 그들은 금속의 염을 형성하는 산과 반응 할 수 있습니다.
세 가지 유형의 금속 산화물이 형성된 알칼리 금속과 알칼리성 지구 금속이 있습니다.
- 산화물 음이온을 함유하는 산화물 (O)
- 과산화물 음이온을 함유하는 과산화물 (O)
- 과산화물 음이온을 함유하는 과산화물. (o 2 )
금속 이온과 결합하는 산소 원자의 수는 금속 이온의 산화 수에 따라 다릅니다. 알칼리 금속은 1가 양이온 만 형성합니다. 따라서 그들은 m 2 만 형성합니다 o 산화물 유형 (여기서 M은 금속 이온이고 O는 산화물 음이온이다). 알칼리성 지구 금속은 이성 양이온을 형성합니다. 따라서 MO 유형 양이온을 형성합니다.

그림 1 :희토류 산화물 - 상단 중심에서 시계 방향 :Praseodymium, Cerium, Lanthanum, Neodymium, Samarium 및 Gadolinium 산화물
알칼리와 알칼리성 지구 금속 산화물은 물과 반응 할 때 수산화물을 형성합니다. 따라서, 그것들은 기본 화합물입니다. D 블록 요소는 산화 상태에 따라 다른 산화물을 형성한다. 예를 들어, 바나듐은 산화 상태 +2, +3, +4 및 +5를 나타냅니다. 따라서, 그것이 형성 할 수있는 산화물은 vo, v 2 입니다 o, vo 2 및 v 2 o 5 .
비 금속 산화물이란 무엇입니까
비금속 산화물은 비금속 원소에 의해 형성된 산화물 화합물입니다. 대부분의 P 블록 요소는 비금속입니다. 그들은 다양한 산화물 화합물을 형성합니다. 비금속 산화물은 산화물 분자를 형성하기 위해 산소 원자와 전자를 공유하기 때문에 공유 화합물입니다.
대부분의 비금속 산화물은 물과 반응 한 후 산을 제공합니다. 따라서, 비금속 산화물은 산성 화합물이다. 예를 들어, so
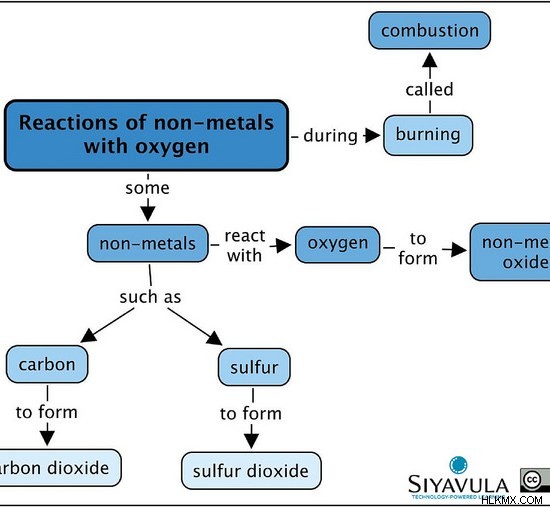
그림 2 :비금속의 산소와의 일부 반응
비금속 산화물은 oxyacids 를 형성 할 수 있습니다 . 옥시 야신은 수용액에서 히드로 늄 이온을 생성한다. 산성 산화물에는 두 가지 유형이 있습니다 :
- 비금속이 N2O5, SO3와 같이 가장 일반적인 산화 상태 중 하나를 나타내는 산산 무수물.
- 비금속이 가장 일반적인 산화 상태를 나타내지 않는 산 산화물. 예 :아니오
2 , clo 2 .
금속 산화물과 비 금속 산화물의 차이
정의
금속 산화물 : 금속 산화물은 금속 및 하나 이상의 산소 원자를 함유하는 화학 화합물입니다.
비 금속 산화물 : 비금속 산화물은 비금속 원소에 의해 형성된 옥사이드 화합물이다.
자연
금속 산화물 : 금속 산화물은 기본 화합물입니다.
비 금속 산화물 : 비금속 산화물은 산성 화합물입니다.
물과의 반응
금속 산화물 : 금속 산화물은 물과 반응하여 기본 용액을 형성합니다.
비 금속 산화물 : 비금속 산화물은 물과 반응하여 산성 용액을 형성합니다.
구조
금속 산화물 : 금속 산화물은 이온 성 화합물입니다. 그러나 산화 상태가 높은 금속 산화물 메타 양이온은 공유 특성을 갖습니다.
비 금속 산화물 : 비금속 산화물은 공유 화합물입니다.
산 및 염기와의 반응
금속 산화물 : 금속 산화물은 산과 반응하여 염을 형성합니다.
비 금속 산화물 : 비금속 산화물은 염기와 반응하여 염을 형성합니다.
결론
금속 산화물은 금속 이온과 산화물 이온으로 구성된 화합물입니다. 비금속 산화물은 비금속 원자 및 산소 원자로 구성된 화합물입니다. 금속 산화물과 비 금속 산화물의 주요 차이점은 금속 산화물이 기본 화합물이고 비금속 산화물은 산성 화합물이라는 것입니다.