핵심 개념
이 튜토리얼에서는 단일 프로토어, 디 프로토, 트리 프로토로 및 다발성 산의 정의를 학습 할 수 있습니다. 또한 여러 산, 다발성 산 내 양성자 사이의 산도 경향과 다발성 산성 곡선 사이의 산도 경향에 대해 배울 것입니다.
다른 기사에서 다루는 주제
- 산 기본 화학
- 강산/염기
- 약산/염기
- 산 및 염기의 특성
- 적정 곡선
어휘
양성자 :이 맥락에서, 양성자는 전자가 제거 된 수소 원자이다 (수소 이온). 또한 h.
를 표시합니다Bronsted-Lowry Acid :양성자 (H) 기증자.
Bronsted-Lowry Base :양성자 (H) 수용체.
k a :산 탈두증 반응에 대한 평형 상수 (전방 방향).
모노 프 로스 산은 란 무엇입니까?
일반적으로 볼 수있는 대부분의 산은 모노 프 로컬이므로 하나의 양성자 만 포기할 수 있습니다. 모노 프 로스 산의 예는 다음과 같습니다.
- HCL (히드로 염산)
- ch 3 COOH (아세트산)
- hno 3 (질산)
염산과 질산은 모두 그들의 공식에 하나의 수소가 있고, 수소는 산성이다 (즉, 양성자로 방출 될 수 있음). 그러나, 아세트산은 산성이 아닌 하이드로겐이 있습니다. 산은 종종 비 생산성 수소를 가질 것임을 주목하는 것이 중요합니다.
다발성산이란 무엇입니까?
다발성 산은 하나 이상의 양성자를 기증 할 수있는 브론 스테드-로운 산이다. 위의 예는 하나의 양성자 만 방출 할 수 있지만, 많은 산은 다수의 산성 수소를 가지고있다. 다음은 몇 가지 예입니다.
- h 2 그래서
4 (황산) - h 3 po 4 (인산)
- c 10 H 16 n 2 o 8 (Ethylenediaminetetraacetic acid 또는 EDTA가 짧음)
이 산산 각각은 하나 이상의 산성 양성자를 갖는다. 황산에는 두 가지가 있으므로 di 라고합니다. protic acid. 인산에는 세 가지가 있으므로 tri 이라고합니다 protic acid. EDTA는 4 개의 산성 양성자를 가지고 있는데, 이는 기술적으로 테라프 성산이라고 불리며 실제로 3 개 이상의 양성자를 갖는 산이 방금 다 프로소스라고 불립니다. 이론적으로, 다 프로소스 산이 가질 수있는 산성 양성자의 수에는 제한이 없다.
다발성산은 어떻게 작동합니까?
산이 양성자를 포기하면 컨쥬 게이트베이스라고 불리는 것을 형성한다는 것을 상기하십시오. 모노 프 성산의 경우, 컨쥬 게이트 염기는 산성 양성자가 없으며 기초로서 (당연히) 작용할 수 있습니다. 그러나, 다발산의 경우, 원래 산의 컨쥬 게이트 염기는 산성 양성자를 갖는다. 즉, 컨쥬 게이트 염기는 또한 산이다. . 몇 가지 예를 살펴 보겠습니다.
HCL ⇌ CL + H
위의 평형에서 강한 단일 염산 인 염산은 산성 수소를 포기합니다. 이것은 컨쥬 게이트 염기, 염화물 및 양성자를 형성합니다. 더 이상 산성 양성자가 없으므로 더 이상 반응이 없습니다.
H 3 po 4 h 2 po 4 + h
상기의 평형은 인산으로부터의 첫 번째 산성 양성자의 손실을 보여준다. 이 양성자가 손실 된 후 컨쥬 게이트 염기에 여전히 산성 양성자가 남아 있습니다 . 이것은 컨쥬 게이트베이스가 다른 평형에서 산으로 작용할 수 있음을 의미합니다.
H 2 po 4 hpo 4 + h
그리고 다시 한번, (두 번째) 컨쥬 게이트 염기에 여전히 산성 양성자가 남아 있습니다. 따라서 발생할 수있는 마지막 탈 양성자가 하나 있습니다.
hpo 4 po po 4 + h
원래 분자 인 인산이 트리 프로토스이기 때문에 방금 발생했던 세 가지 탈모가있었습니다.
트리 프로토 산에서 k a 값이 가장 높습니까?
다발성 산의 산도는 간단합니다. 각 양성자는 마지막 것보다 덜 산성입니다 . 이것은 k a 에 의해 수치 적으로 표현 될 수 있습니다 또는 pk a 각 후속 종의 값. k a 을 상기하십시오 산-염기 반응에 대한 평형 상수입니다 :더 클수록 산이 강해집니다.
H 3 po 4 h 2 po 4 + h k a1 =6.9 x 10
H 2 po 4 hpo 4 + h k a2 =6.2 x 10
hpo 4 po po 4 + h k a3 =4.8 x 10
첫 번째와 두 번째 탈 로토 톤 사이에 k a 거의 5 배 정도 떨어집니다! 이는 첫 번째 양성자가 두 번째 양성자보다 10 만 배 더 산성이라는 것을 의미합니다. 두 번째 및 세 번째 탈 로토 톤 사이에서 k a 5 배 이상 떨어졌습니다. 이것은 인산의 첫 번째 양성자가 세 번째보다 약 100 억 배 더 산성이라는 것을 의미합니다. 일반적으로 외교 또는 트리 프로산에서 마지막 양성자를 제거하는 것은 다소 어렵습니다.
이 표는 많은 다발성을 포함한 다양한 산을 보여줍니다. 스캔을 자유롭게 스캔하고, 모든 다색 산은 더 큰 k a1 를 가지고 있음을 알 수 있습니다. k a2 보다 , 이것은 k a3 보다 큽니다 et cetera. pk a 를 사용하도록 선택한 경우 대신, 더 높은 pk a 를 기억하십시오 값은 k a 의 반대 인 산도가 낮습니다 .
는 단일산보다 강한 디 프로토 산이 더 강합니다.
반드시 그런 것은 아닙니다. 분자에서 산성 수소의 수는 그 수소가 얼마나 산성 인 (또는 구체적으로 가장 산성이 얼마나 산성인지)와 관련이 없습니다. 염산 (모노 프 로스틱)은 인산 (트리 프로토)보다 훨씬 강하고 황산 (디 프로토)은 수경 플루오르 산 (모노 프 로스 성)보다 훨씬 강합니다. 기본적으로, 수소의 수는 차이를 만들지 않습니다.
다 프로 산성 적정 곡선
우리는 polyprotic acid가 첫 번째 양성자를 잃을 때 새로운 약산을 형성한다는 것을 배웠습니다. 이것은 적정을 수행 할 때 기억하는 것이 중요합니다. 아마도 산/염기 화학에서 가장 흔하고 중요한 기술입니다. 새로 형성된 산 (원래 산의 컨쥬 게이트 염기)은 양성자를 잃을 수 있기 때문에, 다발성 산의 적정 곡선은 각각의 산성 양성자에 대해 서로 부착 된 여러 "정상"(모노 프 로스 성) 적정 곡선처럼 보입니다. 강한 염기로 적정하는 디 프로토 산 (예 :황산)을 나타내는 아래의 곡선을 고려하십시오.
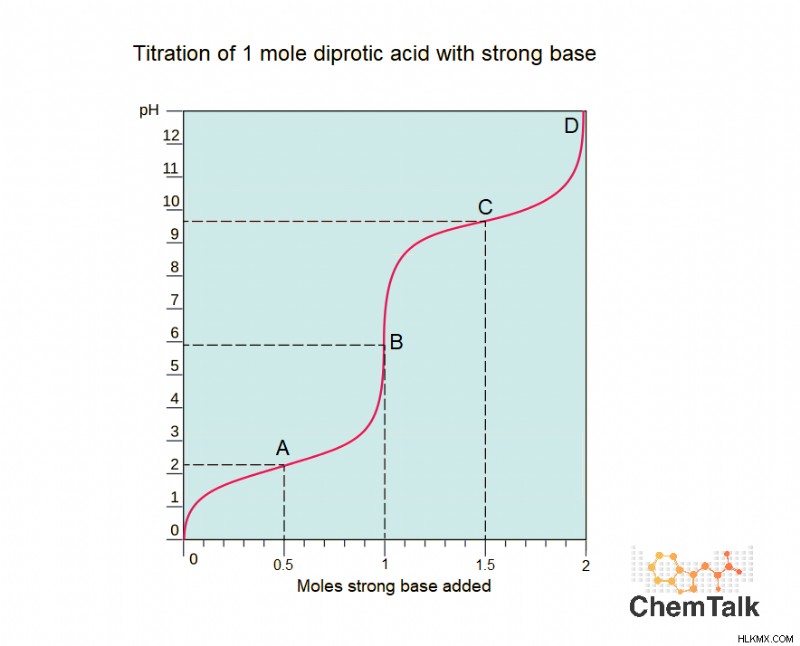
이 곡선에는 a, b, c 및 d.
포인트 A
지점 A에서, 0.5 몰의 염기가 첨가되었는데, 이는 디 프로토 산의 절반이 탈로 톤화되었다는 것을 의미한다. 이것은 산의 절반이 양성자가 남아 있지 않다는 것을 의미합니까? 아니요! 그것은 산의 절반이 하나의 양성자를 잃어 버렸고 여전히 왼쪽을 가지고 있음을 의미합니다. 나머지 절반에는 양성자가 모두 있습니다. 이 시점에서 솔루션은 버퍼입니다. 버퍼 솔루션이 무엇인지 알아 보려면 링크 된 기사를 참조하십시오. 원래 산의 절반이 그의 컨쥬 게이트 염기로 전환 되었기 때문에 용액은 완충제이다. 포인트 A는 두 번째가있을 때 버퍼링 영역, 특히 첫 번째 버퍼링 영역이라고 할 수 있습니다.
포인트 B
B 지점에서 1 몰의 강한베이스가 추가되었습니다. 첫 번째 양성자는 항상 두 번째 양성자보다 더 산성이라는 것을 상기하십시오. 이것은 모든 원래의 산이 첫 번째 양성자와 첫 번째 양성자 만 잃어버린 것을 의미합니다. 점 B는 동등한 점으로 간주됩니다. 하나의 등가 지점 만 갖는 정상 적정과 달리, 다발성 산의 적정은 각각 각각의 연속적인 산성 양성자의 완전한 손실에 해당하는 몇 가지를 가질 것이다.
.포인트 C
이 시점에서 분석 물의 절반은 양성자를 모두 잃어 버렸고 절반은 여전히 왼쪽을 가지고 있습니다. 산과 컨쥬 게이트베이스의 50/50 혼합물이기 때문에 완충액으로 간주됩니다.
점 D
점 D는 두 번째 (및 최종) 등가 지점입니다. D 지점에서, 모든 원래의 산은 완전히 탈 양성자 화되어 염기로 전환되었습니다.
추가 읽기
- PKA
- 평형
- 버퍼 솔루션이란 무엇입니까
- 아이스 테이블 사용