주요 차이 - 칼륨 글루코 네이트 대 클로라이드 칼륨
칼륨은 문자 "k"로 표시되는 화학 요소입니다. 전기 분해에 의해 분리 된 최초의 금속이었습니다. 칼륨은 매우 반응성이며 다양한 비금속 원자와 반응하여 다른 화합물을 형성 할 수 있습니다. 칼륨 글루코 네이트와 염화 칼륨은 두 개의 칼륨 화합물입니다. 칼륨 글루코 네이트는 중요한 칼륨 보충제입니다. 칼륨 글루코 네이트와 염화 칼륨의 주요 차이점은 칼륨 글루코 네이트는 글루코 산의 컨쥬 게이트 염기의 칼륨 염이 반면 염화 칼륨은 칼륨의 금속 할라이드라는 것입니다. .
주요 영역을 다루었습니다
1. 칼륨 글루코 네이트는 무엇입니까
- 정의, 화학 구조 및 특성
2. 염화 칼륨이란 무엇입니까
- 정의, 화학 구조 및 특성
3. 칼륨 글루코 네이트와 염화 칼륨의 유사점은 무엇입니까
- 일반적인 기능의 개요
4. 칼륨 글루코 네이트와 염화 칼륨의 차이점은 무엇입니까?
- 주요 차이점 비교
주요 용어 :전기 분해, 컨쥬 게이트베이스, 글루코 닉 산, IUPAC 이름, KCl, 칼륨, 염화 칼륨, 칼륨 D- 글루코 네이트, 칼륨 글루코 네이트 칼륨

칼륨 글루코 네이트는 무엇입니까
칼륨 글루코 네이트는 글루코 산의 컨쥬 게이트 염기의 칼륨 염입니다. d- 글루콘 산 칼륨 염 라고도합니다 또는 칼륨 d- 글루코 네이트 . 칼륨 글루코 네이트는 체중 16.69% 칼륨으로 구성됩니다. 글루콘 산은 카르 복실 산이다; 따라서, K 이온은 수소 원자를 대체함으로써 하이드 록실기의 산소 원자에 부착된다. 이 화합물은 고체상에 존재합니다. 칼륨 글루코 네이트 칼륨의 융점은 약 175c입니다.
칼륨 글루코 네이트는 흰색 내지 황색 결정 분말 또는 과립으로 이용 가능한 무취 화합물입니다. 약간 식염수 맛이 있습니다. 그것은 물에 용해되며 공기가 안정적입니다. 칼륨 글루코 네이트의 저장 온도는 실온입니다. 이 화합물의 분자 공식은 C 6 입니다 H 11 ko 7 . 칼륨 글루코 네이트의 IUPAC 이름은 칼륨 (2R, 3S, 4R, 5R) -2,3,4,5,6- 펜타 하이드 록시 헤 입니다 .
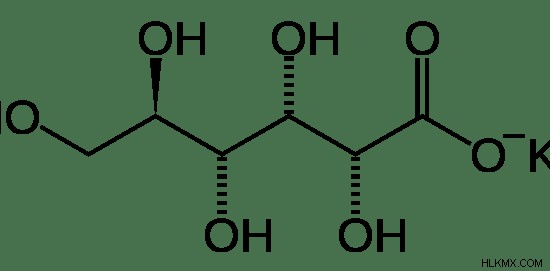
그림 1 :칼륨 글루코 네이트의 화학 구조
칼륨 글루코 네이트는 미네랄 보충제 또는 격리 제로 사용됩니다. 캡슐 또는 벌크 파우더로 판매됩니다. 이 화합물에서, 칼륨 이온 (K)은 이온 결합을 통해 글루코 닉 산의 컨쥬 게이트 염기에 결합된다. 이것은 k와 글루코 네이트 음이온 사이에 정전기 인력이 있음을 의미합니다.
염화 칼륨이란 무엇입니까
염화 칼륨은 화학식 kcl. 를 갖는 금속 할라이드입니다. 무취의 흰색 결정 분말입니다. 그것은 물에 쉽게 녹여 소금 같은 맛을 만듭니다. 비료, 폭발물, 과학적 응용, 식품 가공 등과 같은 많은 용도가 있습니다. KCl은 칼륨과 같은 미네랄에서 생산됩니다.
.KCl의 어금니 질량은 74.548 g/mol입니다. 염화 칼륨의 용액은 강한 식염수 맛을 갖습니다. 염화 칼륨의 융점은 770C이고 끓는점은 1420C입니다. 2732C에서, KCl 결정은 숭고합니다. 따라서 승화 온도입니다. 승화는 액체 상을 거치지 않고 기체상으로 고체를 기화시키는 것이다.
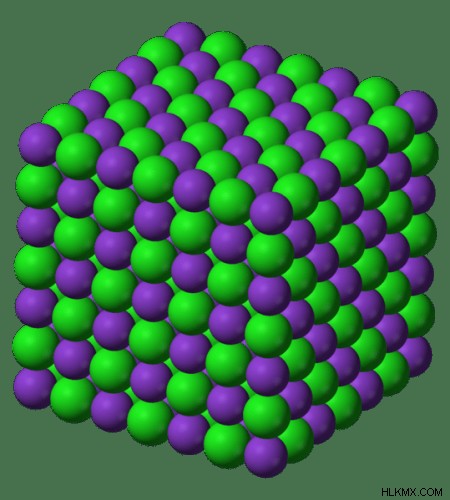
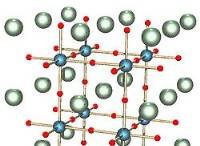
그림 2 :KCl 격자 구조의 다이어그램
kcl은 이온 성 화합물입니다. 작은 칼륨 양이온과 큰 염화물 음이온으로 구성됩니다. KCl의 결정 구조는 NaCl의 결정 구조와 유사하다. 얼굴 중심 입방 단위 세포가 있습니다. KCl 결정은 3 방향으로 쉽게 절단됩니다.
글루코 네이트 칼륨과 염화 칼륨의 유사성
- 둘 다 칼륨 양이온 함유 화합물입니다.
- 둘 다 물에 쉽게 용해됩니다.
- 두 화합물의 용액은 식염수 맛을 갖는다.
칼륨 글루코 네이트와 염화 칼륨의 차이
정의
칼륨 글루코 네이트 : 칼륨 글루코 네이트는 글루코 산의 컨쥬 게이트 염기의 칼륨 염입니다.
염화 칼륨 : 염화 칼륨은 화학식 KCl을 갖는 금속 할라이드입니다.
화학식
칼륨 글루코 네이트 : 칼륨 글루코 네이트의 화학적 공식은 C 6 입니다 H 11 ko 7 .
염화 칼륨 : 염화 칼륨의 화학적 공식은 Kcl.
입니다몰 질량
칼륨 글루코 네이트 : 칼륨 글루코 네이트의 몰 질량은 234.246 g/mol.
입니다염화 칼륨 : 염화 칼륨의 몰 질량은 74.548 g/mol.
입니다용융점 및 끓는점
칼륨 글루코 네이트 : 칼륨 글루코 네이트의 융점은 약 175 ° C입니다.
염화 칼륨 : 염화 칼륨의 융점은 770 ° C이고 끓는점은 1420 ° C입니다. 2732C에서, KCl 결정은 숭고한.
맛
칼륨 글루코 네이트 : 칼륨 글루코 네이트 용액은 약간 식염수 맛을 갖습니다.
염화 칼륨 : 염화 칼륨 용액은 식염수 맛이 강합니다.
승화
칼륨 글루코 네이트 : 칼륨 글루코 네이트는 승화를받지 않습니다.
염화 칼륨 : 염화 칼륨은 승화를 겪을 수 있습니다.
결론
칼륨은 많은 화합물을 형성 할 수있는 반응성이 높은 화학 요소입니다. 칼륨 글루코 네이트 및 염화 칼륨은 이러한 두 화합물입니다. 칼륨 글루코 네이트와 염화 칼륨의 주요 차이점은 칼륨 글루코 네이트 칼륨 글루코 네이트는 글루코 산의 컨쥬 게이트 염기의 칼륨 염이 반면 염화 칼륨은 칼륨의 금속 할라이드라는 것입니다.
.참조 :
1.“칼륨 글루코 네이트.” 국립 생명 공학 정보 센터. Pubchem Compound Database, 미국 국립 의학 도서관, 여기에서 구할 수 있습니다.
2. "염화 칼륨." Wikipedia, Wikimedia Foundation, 2017 년 12 월 31 일.
3. "염화 칼륨." 국립 생명 공학 정보 센터. Pubchem Compound Database, 미국 국립 의학 도서관, 여기에서 구할 수 있습니다.
이미지 제공 :
1. Fvasconcellos의“칼륨 글루코 네이트”01:39, 2007 년 10 월 8 일 (UTC) - Commons Wikimedia2를 통한 자신의 작업 (공개 도메인). Benjah-BMM27의“칼륨 클로라이드 -3D-ionic”-Commons Wikimedia를 통해 자신의 작업 (공개 도메인)