주요 차이 - 아닐린 대 아세타 닐리드
Aniline 및 Acetanilide는 질소 함유 유기 화합물입니다. 그들은 매우 다른 화학적 및 물리적 특성을 가지고 있습니다. 아닐린은 다양한 산업에서 많은 용도를 가지고 있습니다. 아닐린은 아민 기에 부착 된 페닐기로 구성되기 때문에 방향족 아민이다. 아세타 닐리드는 방향족 아미드입니다. 기본이 매우 약하고 염기성은 물보다 훨씬 적습니다. 실온에서 고체 화합물입니다. 아세타 닐리드의 주요 생산 공정은 아세트산 무수물과 아닐린 사이의 반응을 포함한다. 아닐린과 아세타 닐리드의 주요 차이점은 아닐린이 실온에서 황색 고유 한 액체이고 아세타닐 라이트는 흰색에서 회색의 고체 화합물이라는 것입니다.
주요 영역을 다루었습니다
1. aniline
- 정의, 화학적 특성, 생산
2. acetanilide
- 정의, 화학적 특성, 생산
3. 아닐린과 아세타 닐리드의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :아세타 닐리드, 아세트산 무수물, 아미드, 아민 그룹, 암모니아, 아닐린, 안티 라이프 브린, 벤조 나민, 클로로 벤젠, 디아조 늄 염, 수소화, 니트로 벤젠, 질소, N- 페닐 아타 미드 <브로 벤젠

aniline
aniline은 화학식 c 6 를 갖는 질소 함유 유기 화합물입니다. H 7 N. 아민 그룹에 결합 된 페닐기로 구성된다. 벤젠 고리로 구성되기 때문에 아닐린은 방향족 화합물입니다. 아닐린의 주요 용도 중 하나에는 폴리 우레탄 생산을위한 선구자로서의 사용이 포함됩니다.
아닐린의 어금니 질량은 93.129 g/mol입니다. Aniline 은이 화합물에 선호되는 IUPAC 이름이지만 전신 IUPAC 이름은 Benzenamine 입니다. . 실온에서 아닐린은 황색 갈색 액체입니다. 매운 냄새가 나는 지성 액체입니다. 아닐린의 용융점은 -6 ° C이고 끓는점은 184.1 ° C입니다.
aniline은 평면 분자입니다. 그것은 질소 원자에 고독한 쌍이 존재하기 때문에 약한 염기입니다. 아닐린은 니트로 벤젠의 촉매 수소화를 통해 산업적으로 생산된다. 아닐린을 생산할 때, 니트로 벤젠은 50-60C에서 질산과 황산의 혼합물을 사용하여 벤젠 질화로부터 먼저 생산된다. 그런 다음 니트로 벤젠은 금속 촉매의 존재하에 수소화됩니다.

그림 1 :니트로 벤젠의 아닐린 생산
암모니아와 클로로 벤젠 사이의 반응은 아닐린 생산을위한 또 다른 방법입니다. 반응은 다음과 같습니다. 여기서는 특정 온도 및 압력 조건이 필요합니다.
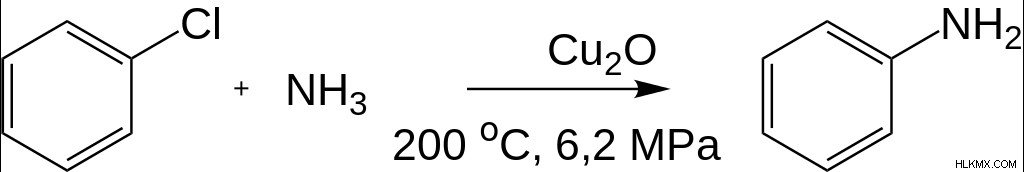
그림 2 :클로로 벤젠의 아닐린 생산
아닐린은 약한 염기이기 때문에 아닐린과 미네랄 산 사이의 반응에서 염을 형성 할 수 있습니다. 산성 배지에서, 디아 조 늄 염은 아닐린과 아질산 간의 반응에 의해 아닐린으로부터 생성 될 수있다. Diazonium salts는 많은 염료 생산에 매우 중요한 구성 요소입니다.
acetanilide
acetanilide는 화학식 c 8 를 갖는 아미드입니다. H 9 아니요. 실온에서, 그것은 무취의 고체 화합물이다. 흰색에서 회색 색상이 있습니다. 아세타 닐리드는 약간 타는 냄새가납니다. 잎 모양의 외관이 있습니다.
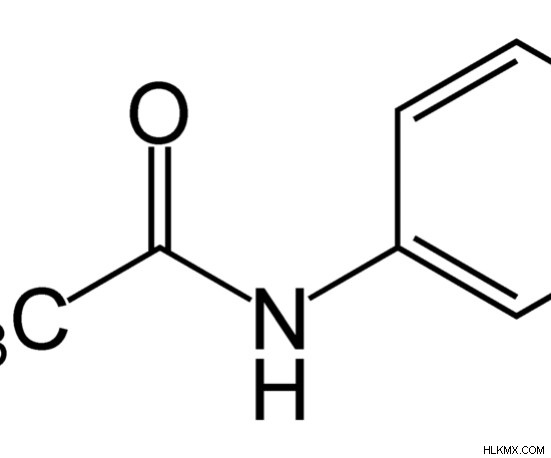
그림 3 :아세타 닐리드의 화학 구조
아세타 닐리드의 몰 질량은 135.166 g/mol입니다. 아세타 닐리드의 융점은 114.3C이고 끓는점은 304C입니다. 이 화합물의 IUPAC 이름은 n 입니다 -페닐 아세트 아미드 . 아세타 닐리드의 상표 이름은 antifebrin 입니다 .
acetanilide는 아세트산 무수물과 아닐린 사이의 반응에 의해 생성 될 수 있습니다. 그러나 생산할 때, 애 리민이 독성이 있고 피부를 통해 흡수 될 수 있기 때문에 반응은 연기 후드 아래에서 수행되어야합니다.
c 6 h 5 nh 2 + (ch 3 CO)
아닐린과 아세타 닐리드의 차이
정의
아닐린 : 아닐린은 화학적 공식을 갖는 질소 함유 유기 화합물이다. H 7 n.
acetanilide : 아세타 닐리드는 화학적 공식 C 8 를 갖는 아미드이다 H 9 아니요.
물리적 상태
아닐린 : 실온에서 아닐린은 지성 액체입니다.
acetanilide : 실온에서 아세타 닐리드는 흰색에서 회색 고체입니다.
몰 질량
아닐린 : 아닐린의 몰 질량은 93.129 g/mol.
이다acetanilide : 아세타 닐리드의 몰 질량은 135.166 g/mol.
이다카테고리
아닐린 : 아닐린은 아민입니다.
acetanilide : 아세타 닐리드는 아미드입니다.
용융점 및 끓는점
아닐린 : 아닐린의 용융점은 -6 ° C이고 끓는점은 184.1 ° C입니다.
acetanilide : 아세타 닐리드의 융점은 114.3C이고 끓는점은 304C입니다.
생산
아닐린 : 아닐린은 니트로 벤젠 또는 클로로 벤젠에서 생산 될 수 있습니다.
acetanilide : 아세타 닐리드는 아닐린에서 생산됩니다.
기초성
아닐린 : 아닐린은 약한 기초입니다.
acetanilide : 아세타 닐리드는 매우 약한 염기입니다.
결론
aniline and acetanilide는 방향족 유기 화합물입니다. 이들 화합물은 기본 화합물이지만 아세타닐 라이트는 아닐린보다 매우 약한 기본이다. 아닐린과 아세타 닐리드의 주요 차이점은 아닐린이 실온에서 황색 고유 한 액체이고 아세타 닐리드는 흰색에서 회색 고체 화합물이라는 것입니다.
참조 :
1.“아닐린.” 국립 생명 공학 정보 센터. Pubchem Compound Database, 미국 국립 의학 도서관, 여기에서 구할 수 있습니다.
2.“아닐린.” Encyclopædia Britannica, Encyclopædia Britannica, Inc. 아닐린으로부터의 아세타 닐리드의 제조, 여기에서 구할 수있다.
이미지 제공 :
1. 영어 Wikipedia의 Navstar의“Aniline Production” - En.wikipedia에서 Commons로 이전. (공개 도메인) Commons Wikimedia
2를 통해. Michał Sobkowski의“클로로벤젠의 아닐린” - Commons Wikimedia
3을 통해 자신의 작업 (공개 도메인).