가스의 압력과 온도 사이의 관계는 게이 -lussac의 압력 온도 법칙에 의해 언급됩니다. 이 법은 일정한 부피로 고정 된 가스 질량의 압력 (p)이 켈빈 온도 (t)에 방향 적으로 비례하다고 명시하고 있습니다. 따라서 특정 시스템의 압력이 높아짐에 따라 해당 시스템의 온도도 올라가고 그 반대도 마찬가지입니다. 가스 법은 압력, 부피, 온도 및 양과 관련하여 가스의 행동을 설명합니다. 가스는 물질의 상태 중 하나이며, 넓은 공간을 채우기 위해 매우 단단히 압축되거나 확장됩니다.
주요 영역이 적용됩니다
1. 압력이란?
- 정의, 가스 압력
2. 온도
- 정의, 측정
3. 압력과 온도의 관계는 무엇입니까
-Gay-Lussac의 법률
주요 용어 :가스, 게이 -Lussac의 법칙, 켈빈, 압력, 온도

압력이란?
압력은 그것과 접촉하는 무언가에 의해 물체에 가해지는 지속적인 물리적 힘입니다. 단위 면적당 힘으로 계산됩니다. 진공으로 둘러싸인 밀폐 된 가스 챔버가 고려 될 때, 챔버 벽의 가스에 의해 가해지는 압력은 세 가지 요인에 의존한다. 그것들은 챔버의 가스량, 챔버의 부피 및 가스의 온도입니다. 다른 파라미터가 일정 할 때, 챔버 내부의 압력은 챔버의 가스량에 직접 비례한다; 챔버의 부피에 반비례합니다. 챔버 내부의 가스 온도에 직접 비례합니다. 압력은 그림 1에서 정의됩니다.
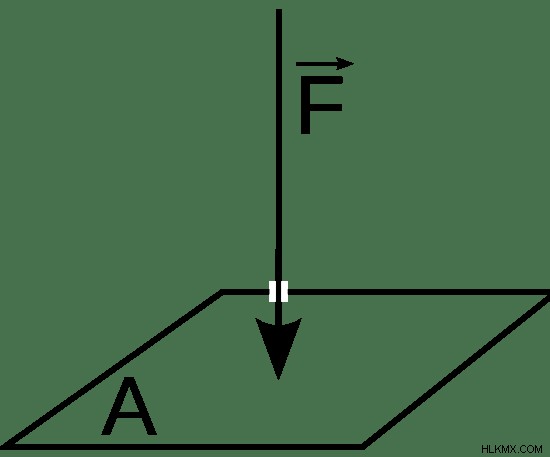
그림 1 :압력
대기압은 우리 위의 공기의 무게로 생성됩니다. 해수면에서는 10 pa입니다.
온도
온도는 물질이나 물체에 존재하는 열 정도입니다. 특정 시스템 내에 포함 된 내부 에너지를 나타냅니다. 온도는 온도계로 측정 할 수 있으며, 이는 다양한 측정 단위로 교정됩니다. 섭씨 스케일은 ° C로 표시되는 온도 측정에 가장 널리 사용되는 척도입니다. 국제 단위 (SI)를 기반으로 한 온도 단위는 켈빈 (k)입니다. 온도계는 그림 2에 나와 있습니다.

그림 2 :온도계
가장 추운 이론적 온도에서 절대 제로 인 경우, 물질에서 입자의 열 운동은 최소입니다. 절대 0은 0 k이고 -273.14 ° C입니다.
압력과 온도의 관계는 무엇입니까
압력과 온도의 관계는 가스와 관련하여 설명됩니다. Gay-Lussac의 법칙은 압력 온도 관계를 설명하는 가스 법입니다. 일정한 부피에서 주어진 양의 특정 가스의 압력은 켈빈 온도에 직접 비례합니다.
로 작성할 수 있습니다- p ∝ t 또는
- p/t =k 여기서 k는 일정하거나
- p 1 /t 1 =p 2 /t 2
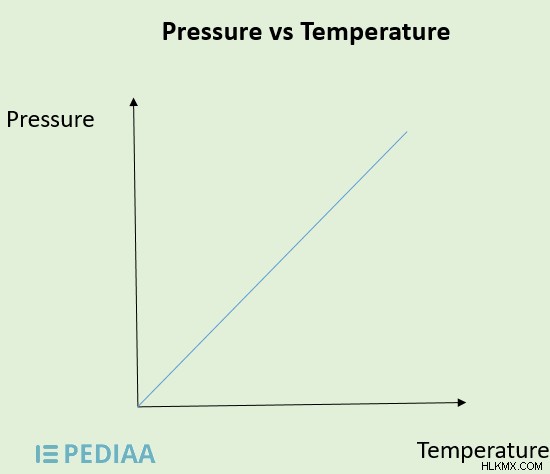
그림 3 :압력과 온도의 관계
특정 시스템의 온도가 증가하면 가스의 분자가 더 빠르게 움직여 가스 용기 벽에 더 큰 압력이 가해집니다. 이것은 시스템의 압력을 증가시킵니다. 시스템의 온도가 감소하면 압력이 줄어 듭니다. 따라서 일정한 부피에서 특정 가스의 압력은 온도에 직접 비례합니다.
결론
주어진 양의 가스의 압력은 주어진 부피에서 온도에 직접 비례합니다. 시스템의 온도가 올라가면 압력도 올라가고 그 반대도 마찬가지입니다. 가스의 압력과 온도 사이의 관계는 게이 -Lussac의 법에 의해 언급됩니다.
참조 :
1.“9.2 압력, 부피, 양 및 온도 관련 :이상적인 가스 법칙.” 화학 , 여기에서 사용할 수 있습니다.
이미지 제공 :
1. Klaus-Dieter Keller의 "압력력 면적"-Commons Wikimedia
2를 통한 자신의 작업 (CC By-SA 3.0). Pixabay를 통한 "1134182"(CC0)