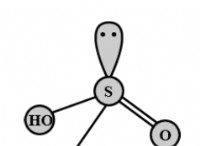
이산화황 및 산소로부터 삼산화황의 형성에 대한 반응은 다음과 같습니다.
$$ 2SO_2 (g) + O_2 (g) \ Rightleftharpoons 2SO_3 (g) $$
Le Chatelier의 원칙에 따르면, 압력을 증가 시키면 몰수 가스가 적은 가스가 적은 평형을 측면으로 이동시킵니다. 이 경우, 삼산화 유물 인 생성물은 2 몰의 가스를 갖는 반면, 반응물 인 이산화황 및 산소는 3 몰의 가스가 있습니다. 따라서, 압력을 증가시키는 것은 삼산화황의 형성에 유리하여 더 높은 수율을 초래할 것이다.
반대로, 압력을 줄이면 반응물의 측면 인 더 많은 두더지 가스로 평형을 측면으로 이동시킵니다. 이것은 삼산화황의 수율을 감소시킵니다.
따라서, 압력을 증가 시키면 트라이 산화 황의 수율이 증가하고 압력을 감소 시키면 수율이 감소합니다.