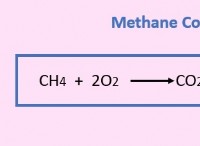
$$ 2li (s) + 2H_2O (L) → 2LIOH (aq) + H_2 (g) $$
이 반응에서, 리튬 금속은 물과 반응하여 리튬 수산화물 및 수소 가스를 형성한다. 반응은 매우 발열 적이며, 이는 상당한 양의 열을 방출한다는 것을 의미합니다. 반응 중에 방출 된 열은 증기 또는 전기를 생성하는 데 사용될 수 있습니다.
리튬은 물과 격렬하게 반응하여 다량의 수소 가스를 방출합니다. 이 반응은 위험 할 수 있으므로 리튬을 처리 할 때 예방 조치를 취하는 것이 중요합니다. 리튬은 항상 잘 통풍이 잘되는 지역에서 처리되어야하며, 물과 접촉 할 수는 없어야합니다.
리튬과 물 사이의 반응은 깨끗한 연소 연료 인 수소 가스를 생산하는 데 사용될 수 있습니다. 수소 가스는 리튬이 물과 반응하여 수산화 리튬 및 수소 가스를 형성 할 때 생산됩니다. 그런 다음 수소 가스를 사용하여 차량 전력을 공급하거나 전기를 생산할 수 있습니다.
리튬과 물 사이의 반응은 청정 에너지를 생산하는 유망한 방법입니다. 그러나이 목적으로 리튬을 사용하는 안전하고 효율적인 방법을 개발하려면 더 많은 연구가 필요합니다.