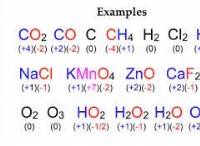
* 원자가 전자 : 이들은 원자의 가장 바깥 쪽 껍질에있는 전자입니다. 그것들은 화학적 결합과 관련된 것입니다.
* 이온 : 이온은 하나 이상의 전자를 얻거나 손실 한 원자 또는 분자로 순 전하를 제공합니다.
연결 :
* 원자가 전자를 얻거나 잃는 것은 이온을 만듭니다. 원자가 전자를 얻을 때, 음이온 (음이온)이됩니다. 전자가 손실되면 양으로 하전됩니다 (양이온). 전자의 이득 또는 손실은 항상 원자가 전자와 관련이 있습니다.
* 원자가 전자는 이온 형성을 결정합니다 : 원자가의 원자가 전자의 수는 안정적인 전자 구성 (고귀한 가스와 같은)을 달성하기 위해 얻거나 잃을 가능성이 얼마나 많은 전자 수를 결정했습니다. 예를 들어, 금속은 원자가 전자가 양이온이되는 경향이있는 반면, 비금속은 음이온이되기 위해 전자를 얻는 경향이 있습니다.
예 :
* 나트륨 (NA) : 나트륨에는 하나의 원자가 전자가 있습니다. 그것은 네온과 같은 안정적인 전자 구성 으로이 전자를 쉽게 잃게됩니다.
* 염소 (CL) : 염소에는 7 개의 원자가 전자가 있습니다. 그것은 아르곤과 같은 안정적인 전자 구성으로 하나의 전자를 클로라이드 이온 (Cl-)으로 얻습니다.
요약 : 원자가 전자는 이온 형성의 주요 업체입니다. 원자가 전자의 수는 원자가 다른 원자와 상호 작용하여 이온과 화학적 결합을 형성하는 방법을 지시합니다.