1. 공식적인 충전을 이해하십시오
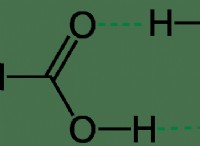
공식 전하는 화학적 결합의 전자가 원자 사이에 동일하게 공유된다고 가정 할 때 분자의 원자에 할당 된 이론적 전하이다. 그것은 분자 내의 전자 분포를 이해하는 데 도움이됩니다.
2. 공식 전하 계산
공식 요금에 대한 공식은 다음과 같습니다.
공식 전하 =(원자가 전자) - (비 결합 전자) - (1/2 * 본딩 전자)
* 원자가 전자 : 원자의 가장 바깥 쪽 쉘에있는 전자의 수.
* 결합 전자 : 결합에 관여하지 않는 전자의 수.
* 결합 전자 : 공유 결합에서 공유되는 전자의 수.
3. CLF 에 적용하십시오
* 염소 (CL) :
* 원자가 전자 :7
* 비 결합 전자 :6 (3 개의 고독 쌍)
* 결합 전자 :2 (단일 결합)
* 공식 전하 =7-6- (1/2 * 2) = 0
* 불소 (f) :
* 원자가 전자 :7
* 비 결합 전자 :6 (3 개의 고독 쌍)
* 결합 전자 :2 (단일 결합)
* 공식 전하 =7-6- (1/2 * 2) = 0
결론
CLF에서 염소 (CL)와 불소 (F)의 공식 전하는 둘 다 0 입니다. . 이것은 전자가 원자 사이에서 비교적 고르게 공유되어 안정적인 분자를 초래한다는 것을 의미합니다.