ha + b ha a⁻ + hb⁺
어디:
* ha 산 입니다 양성자 (H⁺)를 기증합니다.
* b 베이스 입니다 양성자를 받아들입니다.
* a⁻ conjugate base 입니다 산의.
* hb h 컨쥬 게이트 산 입니다 베이스의.
설명 :
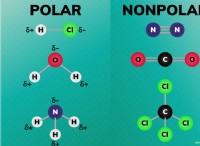
* 산 (ha) :산은 양성자를 기증 할 수있는 물질입니다 (H⁺). 반응에서, HA는 그의 접합체 염기 A⁻를 형성하기 위해 양성자를 잃었다.
* 베이스 (b) :베이스는 양성자 (H⁺)를 수용 할 수있는 물질입니다. 반응에서, B는 산으로부터 양성자를 얻기 위해 그의 공액 산 hb⁺를 형성한다.
중요한 점 :
* 반응은 평형 반응 이다 , 그것은 앞으로 그리고 역 방향으로 진행될 수 있음을 의미합니다.
* 강도 산과 염기의 평형의 위치를 결정합니다. 더 강한 산은 양성자를보다 쉽게 기증하는 반면, 더 강한 염기는 양성자를보다 쉽게 받아들입니다.
* 컨쥬 게이트 산-염기 쌍 항상 평형의 반대쪽에 있습니다.
일반적인 산-염기 반응의 예 :
* HCl (산) + H₂O (염기) ⇌ Cl⁻ (접합체베이스) + H₃O⁺ (Conjugate Acid)
* ch₃cooh (산) + nh₃ (염기) ⇌ ch₃coo⁻ (컨쥬 게이트 염기) + nh₄⁺ (컨쥬 게이트 산)
참고 :
* 일반적인 산-염기 반응은 광범위한 정의 입니다 여기에는 Brønsted-Lowry 이론 및 Lewis 이론과 같은 다양한 산베이스 이론이 포함됩니다.
* 반응의 특정 형태는 관련된 산 및 기초에 따라 다를 수 있습니다.