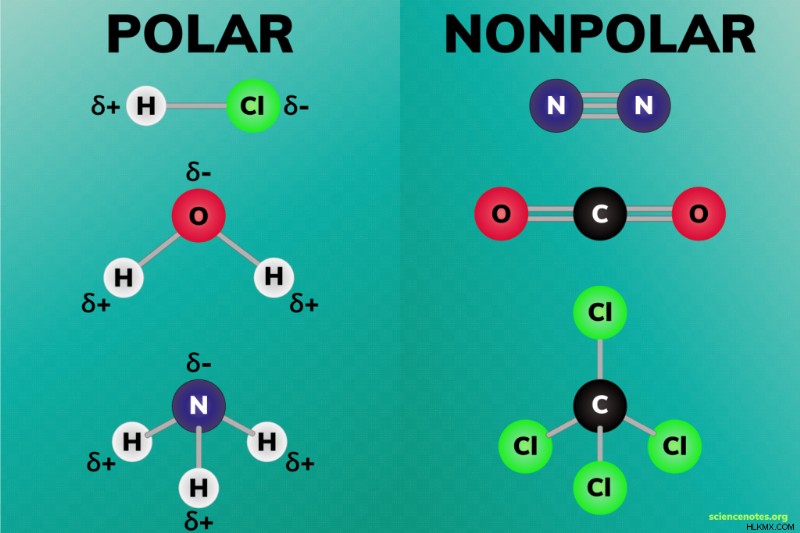
극성 및 비극성 분자는 두 개의 광범위한 분자입니다. 극성은 분자 주변의 전하의 분포를 설명합니다. 전하는 비극성 분자에 골고루 분포되지만 극성 분자에 고르지 않게 분포되어 있습니다. 다시 말해, 극성 분자는 부분 전하의 영역을 가지고 있습니다.
극성 및 비극성 분자의 예는 다음과 같습니다. 극성이 이온 성 및 공유 결합과 어떻게 관련이 있는지, 그리고 극성을 사용하여 어떤 분자가 혼합 할 것인지 예측할 수있는 방법을 살펴 봅니다.
- 비극적 결합은 동일한 전기 음성 값을 가진 두 비금속 사이에 형성됩니다.
- 전기 음성 값이 다른 원소의 원자 사이에 형성됩니다.
- 비극성 분자는 모든 유형의 화학적 결합을 포함 할 수 있지만 부분 전하는 서로를 취소합니다.
- 극성 분자는 극성 공유 또는 이온 결합을 포함하여 부분 전하가 서로를 취소하지 않습니다.
극성 및 비극성 화학 결합
극성 및 비극성 화학적 결합을 이해하고 식별하면 극성 분자를 더 쉽게 이해할 수 있습니다. 극적인 결합에서, 하나의 원자는 부분 양의 전하를 갖는 반면, 다른 원자는 부분 음의 전하를 갖는다. 다시 말해, 극지 결합은 전기 쌍극자를 형성합니다. 비극성 결합에서, 원자는 전자를 동등하게 공유하므로 이들 사이에 부분 양성 또는 음전하가 없다. 원자가 극성 또는 비극성 결합을 형성하는지 여부는 전기 음성 값의 차이에 달려 있습니다.
- 비극적 채권 :비극성 결합은 동일한 전기 음성 값을 갖는 두 원자 사이에 형성됩니다. 이러한 유형의 결합은 순수한 공유 결합입니다. 예를 들어, 두 개의 수소 원자가 비극성 결합을 형성합니다.
- 극지 본드 :두 원자 사이의 전기 음성 값이 가깝지만 동일하지 않은 경우, 원자는 극성 공유 결합을 형성합니다. 극성 공유 결합은 두 개의 상이한 비금속 사이에 형성됩니다. 예를 들어, 수소 (전기 성분 =2.1) 및 염소 (전기 성분 =3.0)는 극성 공유 결합을 형성합니다. 전기 음성 값이 매우 다른 경우, 원자는 이온 결합이라고하는 극성 결합을 형성합니다. 이온 결합은 금속과 비금속 사이에 형성됩니다.
가장 극성 결합은 이온 결합입니다. 극성 공유 결합은 약간 극성입니다. 순수한 공유 결합은 비극성입니다.
극성 분자
극성 분자는 쌍극자를 가지며, 여기서 분자의 일부는 부분 양전하를 가지며 부분은 부분 음전하를 갖는다. 규정형 이온 성 및 극성 공유 분자는 극성 분자이다. 그러나, 2 개 이상의 원자를 함유하는 분자도 극성 일 수있다. 극성 분자는 비대칭 모양, 고독한 전자 쌍 또는 상이한 전기 음성 값을 갖는 다른 원자에 결합 된 중앙 원자를 갖는다. 일반적으로, 극성 분자는 이온 성 또는 극성 공유 결합을 함유한다. 극성 분자의 예는 다음과 같습니다.
- 물 - H 2 o
- 암모니아 - nh 3
- 이산화황 - So
2 - 황화수소 - H 2 s
- 일산화탄소 - Co
- 오존 - O 3
- Hydrofluoric Acid - HF (및 단일 H가있는 다른 분자)
- 에탄올 - C 2 H 6 O (및 한쪽 끝에 OH가있는 다른 알코올)
- 수 크로스 - c 12 H 22 o 11 (및 OH 그룹이있는 다른 설탕)
극성 분자는 종종 친수성 용매에 친수성이며 용해성입니다. 극성 분자는 종종 유사한 몰 질량을 가진 비극성 분자보다 더 높은 융점을 갖는다. 이것은 수소 결합과 같은 극성 분자 사이의 분자간 힘 때문입니다.
비극성 분자
비극성 분자는 전자가 분자의 원자 사이에 동일하게 공유 될 때 또는 분자에서 전자의 배열이 대칭 일 때 쌍극자 전하가 서로를 취소 할 때 형성됩니다. 비극성 분자의 예는 다음과 같습니다.
- 모든 고귀한 가스 :He, NE, AR, KR, XE (기술적으로는 분자가 아닌 원자입니다.)
- homonuclear diatomic 요소의 임의의 모든 것 :h 2 , n 2 , o 2 , cl 2 (이것은 진정으로 비극성 분자입니다.)
- 이산화탄소 - Co 2
- 붕소 Trifluoride - Bf 3
- 벤젠 - C 6 H 6
- 탄소 테트라클로라이드 - CCl 4
- 메탄 - ch 4
- 에틸렌 - C 2 H 4
- 휘발유 및 톨루엔과 같은 탄화수소 액체
- 대부분의 유기 분자, 예외 (알코올 및 설탕과 같은)
비극성 분자는 몇 가지 공통 특성을 공유합니다. 그들은 실온, 소수성에서 물 불용성이며 다른 비극성 화합물을 용해시킬 수 있습니다.
극성 결합을 갖는 비극성 분자
극성은 화학 결합을 형성하는 두 원자 사이의 상대적인 전기성 값에 의존한다. 동일한 전기 음성 값을 갖는 2 개의 원자는 공유 결합을 형성한다. 전자는 공유 결합에서 원자 사이에 골고루 공유되므로 결합은 비극성이됩니다. 약간 다른 전기 음성 값을 갖는 원자는 극성 공유 결합을 형성합니다. 원자 사이의 전기 음성 값이 매우 다를 때, 이온 성 결합이 형성됩니다. 이온 결합은 매우 극성입니다.
종종 결합의 극성은 분자의 극성과 동일합니다. 그러나, 극성 결합과 비극성 결합을 갖는 극성 분자를 가진 비극성 분자가있다! 예를 들어, 붕소 트리 플루오 라이드는 극성 공유 결합을 함유하는 비극성 분자이다. bf 3 붕소와 불소 원자 사이의 결합이 극성이지만 분자 주위에 전하를 골고루 분포하는 삼각 평면 분자이다. 오존은 비극성 공유 결합으로 만들어진 극성 분자의 예입니다. O 3 의 산소 분자 사이의 화학적 결합 원자는 동일한 전기 음성 값을 갖기 때문에 순전히 공유입니다. 그러나 오존 분자는 구부러진 모양 (물과 같은)을 가지며 전자는 세 가지 원자 모두에서 동등한 시간을 소비하지 않습니다. 중간 원자는 부분 양의 전하를 갖는 반면, 두 외부 원자는 각각 부분 음전하를 갖는다.
극성과 오해
극성을 사용하여 2 개의 화합물이 혼잡한지 여부를 예측할 수 있습니다 (용액을 형성하기 위해 혼합 될 것입니다). 경험의 규칙은 "마치 녹는 것처럼"입니다. 이것이 의미하는 바는 극성 용매가 극성 용질을 용해시키는 반면, 비극성 용매는 비극성 용질을 용해 시킨다는 것입니다. 이것은 알코올과 물이 완전히 혼잡 한 이유와 오일과 물이 섞이지 않는 이유를 설명합니다 (극성과 비극성)
한 분자와 다른 분자 사이의 중간 극성을 갖는 화합물은 일반적으로 불용성이있을 때 화학 물질을 용매에 용해시키는 중 사이의 역할을 할 수 있습니다. 예를 들어, 이온 성 또는 극성 화합물을 유기 비극성 용매에 혼합하려면 먼저 에탄올로 용해 될 수 있습니다. 에탄올은 약간 극성이지만 종종 용질을 용해시키기에 충분합니다. 극성 분자가 용해 된 후, 에탄올 용액을 자일렌 또는 벤젠과 같은 비극성 유기 용매에 혼합합니다.
참조
- Ingold, C. K.; Ingold, E. H. (1926). “탄소 사슬에서 교대 효과의 특성. 파트 V. 극성 및 비극성 해리의 각각의 역할에 대한 특별한 참조를 갖는 방향족 치환에 대한 논의; 산소와 질소의 상대적 지침 효율성에 대한 추가 연구”. j. 화학 Soc . :1310–1328. doi :10.1039/jr9262901310
- Mack, Kenneth M.; Muenter, J. S. (1977). “분자 빔 분광법으로부터 오존의 스타크와 제만 특성”. 화학 물리학 저널 . 66 (12) :5278–5283. doi :10.1063/1.433909
- Pauling, L. (1960). 화학 결합의 특성 (제 3 판). 옥스포드 대학 출판부. ISBN 0801403332.
- Ziaei-Moayyed, Maryam; 굿맨, 에드워드; 윌리엄스, 피터 (11 월 1,2000). "극성 액체 스트림의 전기 편향 :오해 된 데모". 화학 교육 저널 . 77 (11) :1520. doi :10.1021/ed077p1520







