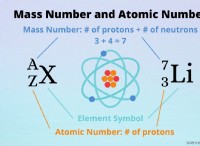
1. 버퍼 시스템을 이해합니다
* 젖산 (HC3H5O3) 약산입니다.
* 나트륨 락 테이트 (NAC3H5O3) 그의 접합체 염기, 젖산 이온 (C3H5O3-)의 염이다.
2. Henderson-Hasselbalch 방정식을 사용하십시오
완충액의 pH는 Henderson-Hasselbalch 방정식에 의해 결정됩니다.
pH =pka + log ([컨쥬 게이트베이스]/[약산])
* pka : 젖산에 대한 산 해리 상수 (KA)의 음성 로그. 이 값은 테이블이나 온라인에서 찾을 수 있습니다. 젖산의 PKA는 대략 3.86입니다.
* [conjugate base] : 젖산 이온의 농도 (C3H5O3-).
* [약산] : 젖산의 농도 (HC3H5O3).
3. 산 및 컨쥬 게이트 염기의 농도를 계산하십시오
* 젖산 :
* 젖산 몰 =(0.085 L) * (0.13 mol/l) =0.01105 mol
* 완충액에서 젖산의 농도 =(0.01105 mol) / (0.085 L + 0.095 L) =0.0614 mol / L
* 젖산 이온 :
* 락 테이트 나트륨 몰 =(0.095 L) * (0.15 mol/l) =0.01425 mol
* 완충액에서 젖산 이온의 농도 =(0.01425 mol) / (0.085 L + 0.095 L) =0.0792 mol / l
4. 값을 방정식 에 연결하십시오
pH =3.86 + 로그 (0.0792 / 0.0614)
pH ≈ 3.86 + 0.11
pH ≈ 3.97
따라서 완충액의 pH는 대략 3.97입니다.