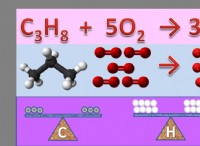
1. 비금속 사이에 형성된 화합물 :
* 이유 : 비금속은 일반적으로 유사한 전기성을 갖는다. 이것은 그들이 전자를 유치하는 경향이 비슷하다는 것을 의미합니다. 두 개의 비금속 결합이있을 때, 전기 음성의 차이는 전자의 완전한 전달을 초래할만큼 충분히 크지 않으며, 이온은 이온 결합에 필요하다. 대신, 그들은 전자를 공유하여 공유 결합을 형성합니다.
* 예 :
* 이산화탄소 (이산화탄소)
* H2O (물)
* NH3 (암모니아)
* CL2 (염소 가스)
* CH4 (메탄)
2. 전기 음성 차이가 낮은 화합물 :
* 이유 : 이온 성 결합은 두 원자, 일반적으로 금속과 비금속 사이의 전기 음성성에 유의 한 차이가있을 때 형성됩니다. 전기 음성 차이가 작을 때, 본드는 본질적으로 더 공유 될 것이다.
* 예 :
* PCL3 (Thophorus trichloride) - 인은 비금속이지만 염소에 비해 전기 음성 성이 상대적으로 낮습니다.
* HI (요오드화 수소) - 요오드는 비금속이지만 전기 음성 불소, 염소 및 브롬보다 전기 음성 성이 낮습니다.
3. 녹고 끓는 점이 높은 화합물 :
* 이유 : 이온 성 화합물은 전형적으로 이온들 사이의 강한 정전기력으로 인해 높은 용융 및 끓는점을 갖는다. 화합물의 융점이 상대적으로 낮 으면 이온 성일 가능성이 적습니다.
* 예 :
* 에탄올 (CH3CH2OH) 및 아세톤 (CH3COCH3)과 같은 많은 유기 화합물
중요한 참고 :
* 극성 공유 결합 : 일부 화합물은 "극성 공유"로 간주되는 결합을 가지고 있으며, 이는 전자가 고르지 않게 공유됩니다. 이러한 결합은 일부 이온 성 특성을 가질 수 있지만 전체 결합은 크게 공유 상태로 남아 있습니다.
더 많은 예를 원하거나 특정 화합물을 탐색하고 싶다면 알려주세요!