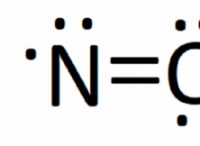반응 :
구리 (Cu)는 질산 (II) 질산염 (Cu (NOA) ₂), 이산화 질소 가스 (NOA) 및 물 (HATE)을 생성하기 위해 질산 (HNOA)과 반응합니다.
균형 화학 방정식은 다음과 같습니다.
Cu + 4hno₃ → Cu (No₃) ₂ + 2no₂ + 2h₂o
설명 :
* 산화제로서의 질산 : 질산은 강한 산화제 역할을한다. 이것은 다른 물질에서 전자를 쉽게 받아들이므로 산화 될 수 있습니다.
* 구리 산화 : 구리는 원소 상태 (cu⁰)에서 구리 (II) 이온 (cu²⁺)으로 산화된다.
* 질소 감소 : 질산의 질소는 hno₃의 +5 산화 상태에서 NOA에서 +4 산화 상태로 감소된다.
* 질산 구리의 형성 : 구리 (II) 이온은 질산염 이온 (NOI)과 결합하여 가용성 화합물 인 구리 (II) 질산염을 형성한다.
* 이산화 질소의 진화 : 질산으로부터의 감소 된 질소 원자는 이산화 질소 가스를 형성하며, 이는 적갈색의 독성 가스입니다.
관찰 :
* 갈색 가스 : 반응은 이산화 질소 인 갈색 가스를 생성합니다 (NOI).
* 블루 솔루션 : 반응이 진행됨에 따라 구리 (II) 질산염의 형성으로 인해 용액이 파란색으로 변한다.
* 열 생산 : 반응은 발열이므로 열이 방출됩니다.
왜 간단한 변위 반응이 아닌가?
구리는 다른 산과 마찬가지로 질산에서 수소를 대체 할 것이라고 생각할 수 있습니다. 그러나, 질산은 강한 산화제이므로, 구리를 감소시키지 않고 산화하는 것을 선호합니다.
추가 메모 :
* 질산의 농도는 반응에 영향을 미칩니다. 농축 질산은 더 많은 이산화 질소 가스를 생산합니다. 희석 질산은 대신 산화 질소 가스 (NO)를 생성합니다.
* 반응은 매우 활발하며, 생산 된 연기는 조심스럽게 처리되어야합니다.
이러한 측면에 대한 자세한 정보를 원하시면 알려주세요!