이것이 중요한 이유는 다음과 같습니다.
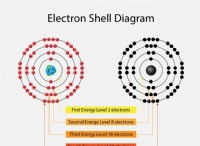
* 안정성 : 전체 외부 껍질은 네온을 엄청나게 안정적으로 만듭니다. 전체 쉘의 전자는 핵에 단단히 결합되어 쉽게 손실되거나 얻지 못합니다. 이것이 네온이 불활성 가스이며 다른 요소와 쉽게 화학적 결합을 형성하지 않는 이유입니다.
* 옥트 규칙 : 네온은 옥트 규칙을 따릅니다.이 규칙은 원자가 외부 쉘에서 8 개의 전자의 안정적인 구성을 달성하기 위해 전자를 얻거나 잃거나 공유하는 경향이 있다고 말합니다. 네온은 이미 외부 쉘 (2s² 2p⁶)에 8 개의 전자를 가지고 있기 때문에이 안정성을 달성하기 위해 다른 원자와 상호 작용할 필요가 없습니다.
* 낮은 반응성 : 네온의 외부 껍질의 안정성은 매우 반응하지 않습니다. 화합물을 쉽게 형성하거나 화학 반응에 참여하지 않습니다. 그렇기 때문에 네온 표시 및 레이저와 같이 불활성이 필요한 응용 분야에서 사용되는 이유입니다.
대조적으로, 부분적으로 채워진 외부 껍질을 갖는 원자는 전자를 얻거나 잃거나 공유함으로써 완전한 외부 껍질을 달성하기 위해 노력하기 때문에 더 반응성이 높은 경향이있다. 그렇기 때문에 나트륨 (외부 껍질의 1 개의 전자) 및 염소 (외부 껍질의 7 개의 전자)와 같은 요소는 반응성이 높고 쉽게 화합물을 형성하는 이유입니다.