1. 핵 :
- 라듐 (RA)의 원자 수는 88이므로 핵에 88 개의 양성자가 있습니다.
- 핵은 또한 중성자를 함유하며, 총 양성자 수와 중성자는 원자 질량을 결정합니다. 라듐의 가장 흔한 동위 원소 인 RA-226은 138 개의 중성자를 가지고 있습니다.
- 핵은 양성자로 인해 긍정적으로 하전됩니다.
2. 전자 껍질 :
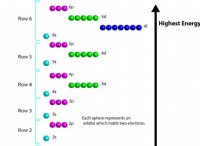
- 전자는 껍질이라는 특정 에너지 수준으로 핵을 공전합니다.
- 각 쉘의 전자 수는 다음 규칙에 의해 결정됩니다. 2n², 여기서 n은 쉘 수입니다.
- 라듐에는 88 개의 전자가 있으며 다음 쉘에 분포되어 있습니다.
- 쉘 1 (k) : 2 개의 전자
- 쉘 2 (l) : 8 전자
- 쉘 3 (m) : 18 전자
- 쉘 4 (n) : 32 전자
- 쉘 5 (O) : 18 전자
- 쉘 6 (P) : 2 개의 전자
- 쉘 7 (Q) : 2 개의 전자
3. 전자 구성 :
- 라듐의 전자 구성은 다음과 같습니다. 1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P⁶ 5S² 4D¹⁰ 5P⁶ 6S² 4F¹⁴ 5D¹⁰ 6P⁶ 7S².
4. 원자가 전자 :
- 가장 바깥 쪽 껍질 인 7S 쉘에는 2 개의 전자가 들어 있습니다. 이들은 화학 결합에 관여하는 라듐의 원자가 전자입니다.
시각적 표현 :
Bohr-Rutherford 모델은 전자 쉘을 나타내는 7 개의 동심원으로 둘러싸인 88 개의 양성자 및 138 개의 중성자를 갖는 중심 핵으로 라듐을 묘사 할 것이다. 각 쉘의 전자 수는 점 또는 작은 원으로 표시됩니다.
한계 :
-Bohr-Rutherford 모델은 단순화 된 표현이며 전자의 양자 특성을 정확하게 설명하지 않습니다.
- 전자의 파도와 같은 특성 또는 특정 공간 영역에서 전자를 찾을 확률을 설명하지 않습니다.
- 전자 스핀의 현상을 설명하지 않습니다.
현대 접근 :
오늘날, 원자 구조를 나타내는 가장 정확한 모델은 양자 기계 모델이며, 이는 더 복잡하지만 원자 행동에 대한 이해를 더 잘 제공합니다.
요약하자면, 라듐의 Bohr-Rutherford 모델은 88 개의 전자 껍질을 함유 한 7 개의 전자 껍질로 둘러싸인 88 개의 양성자 및 138 개의 중성자를 함유 한 양전하 핵을 갖는 원자 구조를 묘사합니다. . 그러나이 모델은 단순화되어 있으며 한계가 있음을 주목하는 것이 중요합니다.