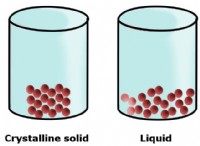
극성 물질은 극성 용매에 용해되고 비극성 물질은 비극성 용매에 용해됩니다.
다음은 고장입니다.
* 극성 물질 전자 밀도의 고르지 않은 분포가있는 분자가 있습니다. 이것은 분자 내에서 전하의 분리를 생성하여 부분 양성 (+) 및 부분 음성 (-) 말단을 형성합니다. 예로는 물 (H (O), 에탄올 (C₂H₅OH) 및 당 (C₁₂H₂₂O₁₁)이 있습니다.
* 비극성 물질 전자 밀도가 고르게 분포 된 분자가 있습니다. 그들은 상당한 전하 분리가 없습니다. 예를 들어 오일, 휘발유 및 지방이 있습니다.
작동 방식 :
극성 물질이 극성 용매에 용해 될 때, 용질 분자의 양의 말단은 용매 분자의 음성 말단에 끌리고, 그 반대도 마찬가지입니다. 이 매력은 용질 분자를 함께 유지하는 힘을 극복하여 용매 전체에 분산시킬 수 있습니다.
유사하게, 비극성 물질은 분자들 사이의 약한 분자간 힘이 유사하기 때문에 비극성 용매에 용해되어 상호 작용하고 혼합 할 수 있기 때문이다.
왜 "좋아요":
열쇠는 분자간 힘의 특성 입니다 . 극성 분자는 더 강한 쌍극자 쌍극자 힘과 수소 결합을 통해 상호 작용합니다. 비극성 분자는 주로 약한 런던 분산 세력을 통해 상호 작용합니다.
유사한 분자간 힘을 가진 물질이 혼합 될 때, 효과적으로 상호 작용하여 용해 될 수 있습니다. 그러나 분자간 힘이 크게 다르면 (극 및 비극성과 같은) 분자 사이의 인력이 약해서 용해되는 것을 방지합니다.
예 :
* 물 (극) 및 소금 (극) : 소금은 둘 다 극성이기 때문에 물에 용해됩니다. 염의 양성 나트륨 이온 (Na⁺)은 물 분자의 음성 산소 말단에 끌리며, 음성 클로라이드 이온 (Cl⁻)은 양성 수소 말단에 끌린다.
* 오일 (비극성) 및 물 (극) : 오일은 극성이 다르기 때문에 물에 녹지 않습니다. 오일 분자 사이의 약한 런던 분산 힘은 물 분자 사이의 강한 수소 결합을 극복하기에 충분히 강하지 않습니다.
결론 :
"좋아요"라는 문구는 용해도를 결정할 때 분자 극성의 중요성을 강조합니다. 이 개념을 이해하는 것은 특히 일상 생활과 화학 반응에서 혼합 될 때 다른 물질의 행동을 예측하는 데 중요합니다.