* 크기 및 전기 음성 : 실리콘은 탄소보다 크고 전기 음성이 적습니다. 이것은 원자가 전자가 핵에서 멀리 떨어져 있고 덜 단단히 고정되어 있음을 의미합니다. 더 작고 전기 음성이 강한 산소는 전자를 자체로 끌어 당겨 실리콘이 이중 결합으로 전자를 공유하기가 더 어렵습니다.
* π- 결합 : 이중 결합은 시그마 본드와 PI 결합의 형성을 포함한다. PI 결합은 p- 궤도의 옆으로 겹치는 것에 의해 형성된다. 실리콘은 더 큰 원자 반경을 가지며, 그 p- 궤도는 강한 π- 결합을 형성하는데 덜 효과적이다.
* d- 궤도 참여 : 실리콘은 빈 D- 궤도를 가지고 있지만 에너지 수준이 높기 때문에 결합에 쉽게 이용할 수 없습니다. 일부 이론은 π- 결합에 d- 궤도 관여를 제안하지만, 다른 요인들에 비해 일반적으로 덜 중요하다고 간주됩니다.
결과 :
* 이산화 실리콘 (SIO2) : 실리콘은 실리콘과 산소 사이의 단일 결합을 갖는 강한 공유 네트워크 구조를 형성한다. 이 네트워크 구조는 이산화 규소에 높은 융점과 경도를 제공합니다.
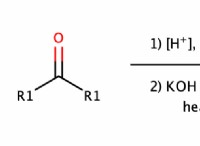
* 실리콘 : 산소로 이중 결합을 형성하는 대신, 실리콘은 산소와 단일 결합을 형성하고 유기 그룹과 결합을 형성합니다. 이로 인해 실리콘이 형성되는데, 이는 고유 한 특성으로 인해 광범위한 응용 분야에서 사용됩니다.
요약하면, 실리콘의 크기, 전기 음성 성 및 안정적인 π- 결합 형성의 어려움은 산소와 이중 결합을 형성하는 것을 방지합니다.