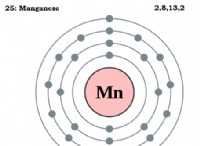
1. 흥분 : 원자는 일반적으로 접지 상태에 있으며 전자는 가장 낮은 에너지 수준을 차지합니다. 에너지가 원자 (예 :열, 전기 또는 빛)에 첨가 될 때 전자는이 에너지를 흡수하고 더 높은 에너지 수준으로 점프합니다. 이것을 excitation 라고합니다 .
2. 이완 : 흥분된 전자는 불안정하고 낮은 에너지 수준으로 돌아 오는 경향이 있습니다. 이 전이는 빛의 형태로 흡수 된 에너지를 방출합니다.
3. 방출 : 방출 된 빛은 흥분 상태와 지상 상태 사이의 에너지 차이에 해당하는 특정 에너지를 가지고 있습니다. 이 에너지는 양자화되므로 개별 값으로 만 존재할 수 있습니다. 각각의 특정 에너지 수준 차이는 고유 한 파장 (및 따라서 색상)의 빛에 해당합니다.
4. 스펙트럼 라인 : 방출 된 빛은 분광기와 같은 장치를 사용하여 구성 요소 파장으로 분리됩니다. 결과는 배출 라인이라는 일련의 밝은 선 입니다. , 어두운 배경에. 이 라인은 여기 원자에 의해 방출되는 빛의 특정 파장을 나타냅니다.
키 포인트 :
* 고유 스펙트럼 : 각 요소에는 지문과 같은 고유 한 원자 방출 스펙트럼이 있습니다. 이를 통해 샘플에 존재하는 요소를 식별 할 수 있습니다.
* 응용 프로그램 : 원자 방출 분광법은 다음을 포함하여 다양한 분야에서 사용됩니다.
* 분석 화학 :샘플에서 요소를 식별하고 정량화합니다.
* 천문학 :별과 행성의 구성을 연구합니다.
* 법의학 :추적 증거 분석.
요약하면, 원자 방출 스펙트럼은 원자의 여기 전자가지면 상태로 돌아올 때 방출 된 에너지로부터 발생하여 각 요소에 고유 한 특정 파장으로 빛을 방출합니다.