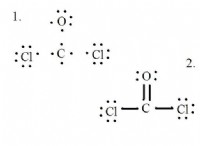br l (l) + h₂o (l) ⇌ hbr (aq) + hobr (aq)
다음은 어떤 일이 발생하는지에 대한 고장입니다.
* 산화 : 하나의 브로민 원자는 전자를 이득하여 HBR에서 브로마이드 이온 (BR-)을 형성한다. 이것은 감소입니다.
* 감소 : 다른 브롬 원자는 전자를 잃어 전자를 잃어 HOBR에서 저소 브로 마이트 이온 (obr-)을 형성한다. 이것은 산화입니다.
중요한 점 :
* 반응은 가역적이므로 평형이 조건에 따라 변할 수 있음을 의미합니다.
* HOBR은 약산 및 강력한 산화제입니다. 그것은 브로민 물의 표백 및 소독 특성을 담당합니다.
* 반응은 과도한 물이 존재함으로써 선호됩니다.
* 브롬 물의 색은 호프 형성으로 인해 주황색 갈색에서 옅은 노란색으로 변합니다.
응용 프로그램 :
이 반응은 다음을 포함한 다양한 응용 분야에서 중요합니다.
* 소독 : 브롬 수는 수영장과 스파에서 소독제로 사용됩니다.
* 표백 : Hobr는 강력한 표백제입니다.
* 유기 합성 : HOBR은 다양한 유기 반응에서 시약으로 사용됩니다.
전반적으로, 브롬과 물 사이의 반응은 복잡하지만 중요한 과정으로 여러 귀중한 화학 종의 형성으로 이어집니다.