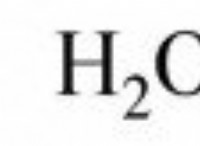1. 핵 전하 : 산소는 수소 (1 양성자)보다 핵 전하 (8 양성자)가 더 높습니다. 이것은 산소 핵이 전자를 더 강력하게 끌어들이는 것을 의미합니다.
2. 전자 껍질의 수 : 산소에는 2 개의 전자 껍질이 있고 수소에는 하나만 있습니다. 이것은 산소의 가장 바깥 쪽 전자가 핵에 더 가깝고 더 강한 매력을 경험한다는 것을 의미합니다.
3. 효과적인 핵 전하 : 산소에서 원자가 전자에 의해 경험되는 효과적인 핵 전하는 수소보다 높다. 산소의 내부 전자는 수소보다 효과적으로 완전 핵 전하에서 원자가 전자를 차폐하기 때문입니다.
4. 원자 크기 : 산소는 수소보다 작습니다. 산소의 크기가 작을수록 원자가 전자가 핵에 더 가깝고 더 강한 정전기 인력을 경험한다는 것을 의미합니다.
5. 전자 구성 : 산소는 2p4 전자 구성을 가지고 있으며, 이는 가장 바깥 쪽 P 궤도에 4 개의 전자가 있습니다. 이들 P 궤도는 수소의 1S 궤도보다 더 확산되고 차폐가 적어 핵에 의해 전자가 더 쉽게 끌린다.
요약 : 산소의 더 높은 핵 전하, 더 작은 크기 및 더 확산 된 전자 구성은 전자에 대한 더 강한 인력을 초래하여 수소에 비해 전기성이 높아집니다.