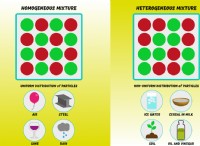
간단한 예 :
* 오존 (O3) :오존의 이중 결합은 3 개의 산소 원자 모두에 대해 비편성됩니다.
* 탄산염 이온 (CO32-) :음전하 및 이중 결합은 세 가지 산소 원자 모두에 대해 비편성됩니다.
* 질산 이온 (No3-) :탄산염과 유사하게, 음전하 및 이중 결합은 3 개의 산소 원자에 대해 비편성됩니다.
더 복잡한 예 :
* 벤젠 (C6H6) :6 개의 탄소 원자는 번갈아 단일 및 이중 결합으로 고리를 형성합니다. 전자는 전체 고리에 비해 분비되어 매우 안정적인 분자를 초래합니다.
* 방향족 화합물 :벤젠과 유사하게, 많은 방향족 화합물은 고리 내의 전자의 비편성으로 인해 공명을 나타냅니다.
* 아미드 (RCONH2) :탄소와 산소 사이의 이중 결합과 질소 원자의 고독한 쌍은 탄소, 산소 및 질소 원자에 대해 비편 화된다.
공명에 대한 핵심 사항 :
* 박대 된 전자 :공명은 전자가 두 특정 원자 사이에 국한되지 않지만 여러 원자에 퍼질 때 발생합니다.
* 하이브리드 구조 :공명을 나타내는 분자의 실제 구조는 가능한 모든 기여 공명 구조의 하이브리드입니다. 이것은 종종 기여 구조 사이의 이중 머리 화살표로 표시됩니다.
* 안정성 증가 :공명은 일반적으로 전자가 넓은 영역에 퍼져 있기 때문에 일반적으로 분자의 안정성을 증가시킨다.
분자가 공명을 나타내는 지 확인하는 방법 :
* 교대 단일 및 이중 채권을 찾으십시오 :이것은 공명의 일반적인 지표입니다.
* 고독한 쌍을 가진 원자를 식별하십시오 :고독한 쌍은 공명에 참여할 수 있습니다.
* 양수 또는 음전하를 확인하십시오 :요금은 또한 비편정 될 수 있습니다.
이것들은 단지 예일 뿐이며 공명을 나타내는 다른 분자가 많이 있습니다. 특정 분자가 공명을 나타내는 지 확실하지 않은 경우 위에서 언급 한 요인을 고려하십시오.