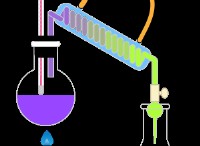
균형 화학 방정식은 다음과 같습니다.
ca (OH) ₂ (aq) + co₂ (g) → caco₃ (s) + h₂o (l)
설명 :
* 이중 변위 : 반응은 두 반응물 사이의 이온 교환을 포함한다. 수산화 칼슘은 칼슘 이온 (Ca²⁺) 및 수산화 이온 (OHA)을 제공하는 반면, 이산화탄소는 수소 이온 (HAT) 및 탄산염 이온 (CO₃²A)을 제공하는 용액에서 탄산 (HATCO)을 형성합니다.
* 중화 : 이 반응은 또한 염기 (수산화 칼슘)가 산성 산화물 (이산화탄소)과 반응하여 염 (탄산 칼슘) 및 물을 형성하기 때문에 중화 반응으로 분류된다.
실제 응용 :
이 반응에는 몇 가지 실제 적용이 있습니다.
* Limewater Test : 반응은 이산화탄소의 존재를 감지하는 데 사용됩니다. 불용성 칼슘 탄산염의 형성으로 인해 이산화탄소가 거품이 생길 때 Limewater (수산화 칼슘의 희석액)가 유백색으로 변합니다.
* 탄산 칼슘 생산 : 이 반응은 시멘트, 건축 자재 및 기타 제품의 핵심 성분 인 탄산 칼슘의 산업 생산에 사용됩니다.
* 산성 토양 치료 : 수산화 칼슘은 산성 토양을 중화시키고 pH를 증가시키고 생식력을 향상시키는 데 사용될 수 있습니다.