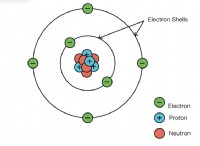
* 공유 결합 원자 사이에 전자 공유를 포함합니다. 이 공유는 단단히 포장 된 구조로 원자를 함께 유지하는 강한 결합을 만듭니다. 공유 결합의 전자는 원자에 단단히 결합되며 자유롭게 이동할 수 없습니다. 이러한 자유 전자의 부족은 재료를 전기의 흐름에 저항하는데, 이는 절연체의 정의 특성입니다.
* 이온 결합 반면에, 한 원자에서 다른 원자에서 다른 원자로 전자를 전달하여 반대 전하로 이온을 생성합니다. 이온 성 화합물은 고체 일 수 있지만, 이온의 하전 된 특성은 약간 전기 전도성을 허용한다.
* 금속 결합 재료 전체에 자유롭게 움직일 수있는 전자의 "바다"를 포함하여 금속이 우수한 전기 도체를 만듭니다.
예 :
* 다이아몬드 : 공유 결합이 강한 탄소 원자로 만들어진 공유 네트워크 고체.
* 고무 : 공유 결합 탄소 원자의 긴 사슬을 갖는 중합체.
* 유리 : 공유 결합 실리콘 및 산소 원자 네트워크를 갖는 비정부 고체.
중요한 참고 : 공유 결합은 절연체에서 가장 일반적인 유형의 결합이지만 예외가 있습니다. 이온 결합이있는 일부 물질은 구조가 이온의 움직임을 방지하는 경우 절연체 역할을 할 수 있습니다.