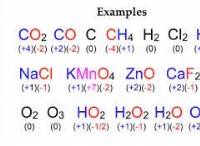
다음은 반응 과정의 고장과 몇 가지 예입니다.
반응 과정 :
* Bromine (BR2)은 규조토 분자입니다. 그것은 실온에서 적갈색 액체로 존재하며 적갈색 가스를 형성하기 위해 쉽게 기화됩니다.
* 금속은 전자를 잃는 경향이 있습니다 양으로 하전 된 이온 (양이온)을 형성합니다.
* 브로민 원자는 전자를 얻는다 브로마이드 이온 (Br-)이라고하는 음으로 하전 된 이온 (음이온)을 형성합니다.
* 금속 양이온 및 브로마이드 음이온은 결합 이온 성 화합물을 형성하기 위해 금속 브로마이드.
예 :
* 나트륨 (NA) + 브로민 (BR2) → 나트륨 브로마이드 (NABR) : 이 반응은 매우 발열 적이며 흰색의 결정질 고체를 생성합니다.
* 철 (Fe) + Bromine (BR2) → 철 (III) 브로마이드 (2 월) : 이 반응은 가열이 시작되기 위해 가열이 필요하지만 발열 성이다. 철 (III) 브로마이드는 적갈색으로 단단합니다.
* 알루미늄 (Al) + Bromine (BR2) → 알루미늄 브로마이드 (ALBR3) : 이 반응은 매우 활발하고 많은 열을 방출합니다. 알루미늄 브로마이드는 흰색의 결정질 고체입니다.
반응성에 영향을 미치는 요인 :
* 금속의 특성 : 나트륨 및 칼륨과 같은 더 반응성 금속은 금이나 백금과 같은 반응성 금속보다 브롬과 더 쉽게 반응합니다.
* 온도 : 온도를 높이면 일반적으로 반응 속도가 높아집니다.
* 촉매의 존재 : 일부 촉매는 금속과 브롬 사이의 반응을 촉진 할 수 있습니다.
안전 고려 사항 :
브롬은 부식성 및 독성 물질입니다. 주의를 기울이고 환기가 잘되는 지역에서 처리하는 것이 중요합니다. 브롬과 관련된 반응은 증기에 대한 노출을 방지하기 위해 연기 후드에서 수행되어야합니다.
요약 :
브롬은 금속과 반응하여 발열 반응에서 금속 브로마이드를 형성한다. 브롬과 금속의 반응성은 금속의 반응성과 반응 조건에 따라 다릅니다. 부식성과 독성 특성으로 인해 항상 브롬을 조심스럽게 처리하십시오.