다음은 다음과 같습니다.
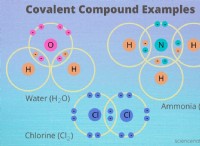
크롬 (CR)은 염산 (HCL)과 반응하여 크롬 (II) 클로라이드 (CRCL) 및 수소 가스 (HAT)를 생성합니다. .
균형 화학 방정식은 다음과 같습니다.
cr (s) + 2hcl (aq) → crcl₂ (aq) + h₂ (g)
설명 :
* 크롬 (CR) 금속이며 수소보다 반응성이 높습니다.
* 염산 (HCl) 수소 이온을 제공하는 강산입니다 (HAT).
* 크롬 (II) 클로라이드 (CRCL₂) 크롬 원자가 전자를 잃어 cr² ⁺ 이온이되기 위해 전자를 잃은 다음 산으로부터의 클로라이드 이온 (cl⁻)과 결합함에 따라 형성된다.
* 수소 가스 (H₂) 수소 이온이 전자를 얻고 결합하여 규정형 수소 분자를 형성함에 따라 생성됩니다.
중요한 참고 :
*이 반응은 단일 변위 반응의 예입니다.
* 반응은 발열 성이므로 열이 방출됩니다.
* 정확한 조건과 제품은 산의 농도와 온도에 따라 달라질 수 있습니다.
다른 질문이 있으면 알려주세요!