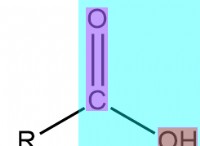
끓는점 이해
* 끓는점 액체가 가스로 변하는 온도입니다.
* 분자 크기 및 분자간 힘 끓는점에 영향을 미칩니다. 더 큰 분자와 더 강한 분자간 힘은 더 높은 비등점을 초래합니다.
에틸 아세테이트와 부틸 아세테이트 비교
* 에틸 아세테이트 (CH3COOCH2CH3) : 끓는점 =77.1 ° C
* 부틸 아세테이트 (CH3COOCH2CH2CH2CH3) : 끓는점 =126.1 ° C
추론
부틸 아세테이트는 에틸 아세테이트보다 끓는점이 상당히 높다. 이것은 다음과 같습니다.
* 부틸 아세테이트는 더 큽니다 : 탄소 사슬이 더 길어 분자 크기와 반 데르 발스 힘 (약한 분자간 명소)을 증가시킵니다.
* 부틸 아세테이트는 더 큰 표면적을 갖는다 : 이것은 또 다른 유형의 약한 분자간 매력, 런던 분산 힘이 더 강해집니다.
결론
순수한 액체가 77.1 ° C에 가까운 비등점이 있다면 에틸 아세테이트 일 가능성이 높습니다. 126.1 ° C에 가까워지면 부틸 아세테이트 일 가능성이 높습니다.
중요한 참고 : 이 분석은 액체가 순수하다고 가정합니다. 불순물은 끓는점에 크게 영향을 줄 수 있습니다.