이유는 다음과 같습니다.
* 이온 성 화합물 및 전도도 : 이온 성 화합물은 양으로 하전 된 이온 (양이온) 및 음이온 (음이온)으로 구성됩니다. 이들 이온은 결정 격자 구조에서 강한 정전기력에 의해 함께 유지된다.
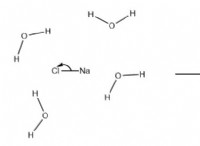
* 물에 용해 : 이온 성 화합물이 물에 용해 될 때, 물 분자는 이온을 둘러싸고 이온 결합을 분리합니다. 이 과정을 해리 라고합니다 . 이온은 용액에서 자유롭게 움직일 수있게됩니다.
* 전기 전기 : 물질이 전기를 전도하려면 자유롭게 움직이는 하전 입자 (이온과 같은)가 필요합니다. 이온 성 화합물이 물에 용해 될 때, 해리 된 이온은 전류를 운반 할 수있다.
따라서 용해 된 이온 성 화합물은 우수한 전기 도체입니다.
예 : 테이블 소금 (NaCl)은 이온 성 화합물입니다. 물에 용해되면 Na+ 및 클리온으로 분리됩니다. 이 이온은 솔루션이 전기를 전도 할 수 있도록합니다.