반응 :
수화 된 탄산나트륨과 염산 사이의 반응은 중화 반응입니다.
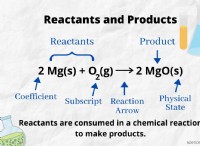
na₂co₂ · xh₂o + 2hcl → 2naCl + (x + 1) H₂O + Co₂
끓는 이유가 필요한 이유 :
* 완전한 반응 : 이 반응은 이산화탄소 가스 (CO₂)를 생성하며, 이는 물에 약간 용해됩니다. 혼합물을 끓여서, 당신은 co₂ 가스를 운전하여 반응을 방해하지 않고 반응이 완료되지 않도록합니다.
* co₂의 제거 : 용액에서 COS의 존재는 반응에서 생성 된 수산화 나트륨 (NaOH)과 반응하여 부정확 한 결과를 초래할 수있는 탄산산 (H주)의 형성으로 이어질 것이다.
* 물의 증발 : 혼합물을 끓여서 과도한 물을 증발시켜 용액을 집중시키고 처리하고 분석 할 수 있도록 도와줍니다.
중요한 메모 :
* 초과 hcl : 과도한 염산의 사용은 모든 탄산나트륨이 완전히 반응하도록하기 위해 중요합니다.
* 안전 : 부식성 연기를 생성 할 수 있으므로 혼합물을 끓일 때주의하십시오. 환기가 잘되는 지역에서 실험을 수행하고 적절한 안전 장비를 착용하는 것이 필수적입니다.
결론적으로, 반응 후 혼합물을 끓여서 완전한 반응을 보장하고, 남아있는 COS를 제거하고, 용액을 집중시킨다. 이것은 정확한 분석에 필수적이며 결과에 영향을 줄 수있는 부작용을 예방하는 데 필수적입니다.