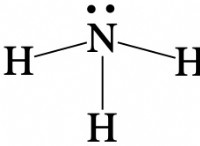
1. 극성 :
* 물은 고도로 극성 분자이므로 전자의 고르지 않은 분포로 인해 양수 및 음성이 있습니다.
* 나트륨 브로마이드는 이온 성 화합물이며, 이는 양으로 하전 된 나트륨 이온 (Na+) 및 음으로 하전 된 브로마이드 이온 (BR-)으로 구성됩니다.
2. 이온 다이폴 상호 작용 :
* 나트륨 브로마이드가 물에 첨가 될 때, 물 분자 (수소 원자)의 양의 끝이 음으로 하전 된 브로마이드 이온에 끌린다.
마찬가지로, 물 분자 (산소 원자)의 음성 끝은 양으로 하전 된 나트륨 이온에 끌린다.
* 이온-쌍극자 상호 작용으로 알려진 이온과 물 분자 사이의 이러한 강력한 관광 명소는 이온을 브로마이드 나트륨의 결정 격자에서 함께 고정시키는 매력적인 힘을 극복합니다.
3. 수화 :
* 이온-다이폴 상호 작용의 결과로, 물 분자는 나트륨과 브로마이드 이온을 둘러싸고 효과적으로 서로 분리됩니다. 이 과정을 수화라고합니다.
* 수화 된 이온은 이제 용액에서 자유롭게 움직일 수있어 브로마이드 나트륨을 물에 용해시킵니다.
4. 엔트로피 :
* 물에 브로마이드 나트륨을 용해시키는 과정은 또한 시스템의 엔트로피 (장애)를 증가시킨다. 엔트로피의 이러한 증가는 열역학적으로 유리한 공정으로 용해도에 기여합니다.
요약하면, 극지수 분자와 브로마이드 나트륨 이온 사이의 강한 이온 다이폴 상호 작용은 엔트로피의 증가와 함께 이온을 고체 상태로 유지하는 격자 에너지를 극복하여 물의 용해도를 초래한다.