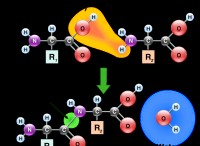
과정 이해
* Naoh는 강력한 기초입니다. 이것은 물과 격렬하게 반응하여 열을 방출하고 많은 열을 생성한다는 것을 의미합니다.
* 안전은 가장 중요합니다 : NAOH를 처리 할 때 항상 적절한 안전 장비 (장갑, 고글, 실험실 코트)를 착용하십시오.
* 느리고 통제 된 추가 : Naoh를 물에 너무 빨리 추가하면 폭력적인 반응이 발생하여 용액을 뿌릴 수 있습니다.
계산 및 절차
1. Naoh의 질량을 계산합니다 :
* NaOH의 몰 질량 =40 g/mol
* 2 몰의 NAOH =2 몰의 질량 * 40 g/mol =80 g
2. 물 준비 :
* 6kg (6000 g)의 물을 측정하십시오.
3. 용해 :
* 느린 추가 : NaOH가 6kg의 물에 80g의 Naoh를 천천히 첨가하여 NAOH가 균등하게 녹을 수 있도록 지속적으로 저어줍니다.
* 열 방출 : NAOH가 녹 으면서 솔루션은 크게 가열됩니다. 진행하기 전에 식히십시오.
4. 농도 (선택 사항) :
* 솔루션의 농도를 알아야하는 경우 다음과 같이 계산할 수 있습니다.
* Molarity (m) : 용액의 두더지 / 용액 부피 (리터)
* NAOH를 녹인 후 솔루션의 최종 볼륨을 알아야합니다. 용해로 인해 솔루션이 부피를 약간 변경할 수 있으므로 신중하게 측정해야합니다.
중요한 메모 :
* 발열 반응 : NaOH의 용해는 매우 발열 적이다. 튀는 것을 방지하기 위해 충분한 컨테이너를 사용하십시오.
* 적절한 처분 : NAOH 솔루션은 위험합니다. 실험실의 안전 프로토콜에 따라 폐기하십시오.
다른 질문이 있으면 알려주세요!