옥트 규칙
옥트 규칙은 원자가 가장 바깥 쪽 쉘 (원자가 쉘)에 8 개의 전자를 갖는 안정적인 전자 구성을 달성하기 위해 전자를 얻거나 잃거나 공유하는 경향이 있다고 명시한다. 이 안정적인 구성은 고귀한 가스의 전자 구성과 유사하며, 이는 전체 원자가 껍질로 인해 매우 반응하지 않습니다.
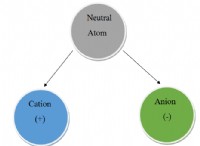
옥트 규칙이 이온에 적용되는 방법 :
* 양이온 : 금속은 안정적인 낙지를 달성하기 위해 전자를 잃는 경향이 있습니다. 예를 들어, 나트륨 (NA)은 하나의 전자를 잃어 Na+가되어 네온 (NE)과 같은 전자 구성으로 양이온을 형성합니다.
* 음이온 : 비금속은 안정적인 옥셋을 달성하기 위해 전자를 얻는 경향이있다. 예를 들어, 염소 (Cl)는 하나의 전자를 얻기 위해 Cl-가되어 아르곤 (AR)과 같은 전자 구성을 갖는 음이온을 형성합니다.
옥트 규칙에 대한 예외 :
옥트 규칙은 유용한 지침이지만 예외가 있습니다.
* 기간 1과 2의 요소 : 이 요소는 최대 바깥 쪽 쉘 (예 :헬륨, 리튬, 베릴륨)에 최대 2 개의 전자 만 담을 수 있습니다.
* 전이 금속 : 전이 금속은 종종 외부 껍질에 8 미만의 전자를 갖는 이온을 형성합니다.
* 기간 3 이상의 요소 : 더 큰 요소는 때때로 가장 바깥 쪽 쉘에서 8 개 이상의 전자를 수용 할 수 있습니다.
요약 :
옥트 규칙은 원자와 이온의 안정성과 반응성을 설명하는 기본 원칙입니다. 안정적인 고귀한 가스 형 구성을 달성하려는 경향에 따라 이온의 전하 및 전자 구성을 예측하는 데 도움이됩니다.