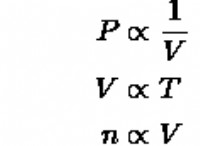다음은 어떤 일이 발생하는지에 대한 고장입니다.
1. 반응물 :
* 질소 가스 (n <<서브> 2 )는 질소 원자 사이의 강한 트리플 결합으로 인해 매우 안정적인 분자입니다.
* 수소 가스 (H 2 )는 또한 비교적 안정적이지만, 그 결합은 질소 트리플 결합보다 약합니다.
2. 반응 조건 :
* 고온 : 반응은 활성화 에너지 장벽을 극복하기 위해 고온 (약 400-500 ℃)이 필요하다.
* 고압 : 고압 (약 200 대기)을 사용하여 반응물의 농도를 증가시켜 암모니아의 형성을 선호합니다.
* 촉매 : 전형적으로 소량의 다른 요소를 갖는 산화철, 촉매는 반응의 속도를 높이기 위해 사용된다.
3. 화학 반응 :
전체 반응은이 방정식으로 표시됩니다.
```
n 2 (g) + 3H 2 (g) <=> 2NH 3 (g)
```
이 방정식은 하나의 질소 분자가 3 개의 분자의 수소와 반응하여 두 분자의 암모니아를 생성 함을 보여준다. 반응은 가역적이므로 암모니아는 다른 조건에서 질소와 수소로 다시 분해 될 수 있음을 의미합니다.
4. 평형 :
반응은 평형에 도달하며, 여기서 암모니아 형성 속도는 암모니아 분해 속도와 같다. 암모니아 생성을 최대화하기 위해, 반응 조건은 신중하게 제어되어 평형을 생성물쪽으로 이동시킨다.
5. 암모니아 형성 :
생산 된 암모니아는 매운 냄새가 나는 무색 가스입니다. 압력으로 쉽게 액화되어 보관하고 운송하기가 더 쉬워집니다.
요약 :
질소 가스와 수소 가스와 암모니아를 형성하는 반응은 고온, 고압 및 촉매를 포함하는 복잡한 과정입니다. 이 반응은 비료 및 기타 산업에서 중요한 성분 인 암모니아를 생산하는 데 중요합니다.