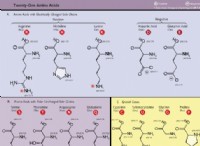
* 원자가 전자 : 붕소와 알루미늄 모두 3 개의 원자가 전자 를 갖는다 가장 바깥 에너지 수준에서. 이것은주기적인 표의 그룹 13 (또는 IIIA)에 있기 때문입니다.
* 전자 구성 : 전자 구성은 비슷한 패턴을 공유합니다.
* 붕소 :1S² 2S² 2P¹
* 알루미늄 :1S² 2S² 2P⁶ 3S² 3P¹
* 양이온을 형성하는 경향 : 두 요소 모두 3 개의 원자가 전자를 잃어 +3 양이온을 형성하는 경향이 있습니다 (b³⁺ 및 al³⁺). 이 전자를 잃어 버리면 가장 바깥 쪽 쉘에서 안정적인 옥켓 전자 구성을 달성 할 수 있기 때문입니다.
그러나 몇 가지 주요 차이점도 있습니다 :
* 에너지 수준 : 알루미늄은 핵에 양성자가 많기 때문에 붕소보다 에너지 수준이 더 많아서 원자 반경이 더 커집니다.
* 금속 문자 : 알루미늄은 금속이고 붕소는 메탈 로이드입니다. 금속 특성의 이러한 차이는 에너지 수준의 수와 결과적 인 전기 음성의 차이에서 비롯됩니다.
요약 : 붕소와 알루미늄은 원자가 전자 수와 +3 양이온을 형성하는 경향이 비슷합니다. 그러나 전체 전자 구성, 에너지 수준 및 금속 특성이 다릅니다.