연료 + 산화제 → 제품 + 열 + 빛
예를 들어 메탄 (천연 가스)의 연소를 사용하는보다 구체적인 예는 다음과 같습니다.
ch meth (메탄) + 2o₂ (산소) → Co₂ (이산화탄소) + 2h₂o (물) + 열 + 빛 >
연소에 대한 핵심 사항 :
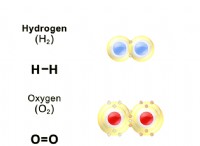
* 연료 : 이것은 화상을 입는 물질, 일반적으로 메탄, 목재 또는 에탄올과 같은 탄화수소입니다.
* 산화제 : 이것은 일반적으로 산소이지만 염소 나 불소와 같은 다른 물질 일 수 있습니다.
* 제품 : 이들은 반응 동안 형성된 물질이다. 탄화수소의 완전한 연소의 경우, 1 차 생성물은 이산화탄소 및 물입니다.
* 열과 빛 : 연소는 열과 빛의 형태로 에너지를 방출하며, 이는 불꽃으로 인식합니다.
연소 유형 :
* 완전한 연소 : 이것은 연료가 완전히 반응하기에 충분한 산소가있을 때 발생하여, 이산화탄소와 물을 1 차 제품으로 생산합니다.
* 불완전한 연소 : 이것은 산소가 제한되어있을 때 발생하여 이산화탄소 및 물과 함께 일산화탄소 (CO) 및 그을음 (탄소 입자)이 형성됩니다. 불완전한 연소는 덜 효율적이며 독성 가스 인 일산화탄소의 생산으로 인해 위험 할 수 있습니다.
연소는 발전소의 전기 생성에서 음식 요리에 이르기까지 광범위한 응용 분야의 기본 화학 반응입니다. 과정과 뉘앙스를 이해하는 것은 에너지 사용을 최적화하고 환경 영향을 최소화하는 데 필수적입니다.