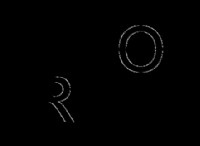
이유는 다음과 같습니다.
* 금속 이온화 에너지가 낮은 경향이 있으며, 이는 전자를 쉽게 잃어 긍정적으로 하전 된 이온 (양이온)을 형성한다는 것을 의미합니다.
* 비금속 전기성이 높은 경향이있는 경향이 있으며, 이는 전자를 쉽게 얻어 음의 하전 이온 (음이온)을 형성한다는 것을 의미합니다.
금속 및 비금속이 반응 할 때, 금속 원자는 전자를 비금속 원자로 잃어서 반대로 하전 된 이온 사이에 정전기 인력을 만듭니다. 이 매력은 화합물을 함께 유지하는 것입니다.
일반적인 이온 성 화합물 쌍의 예 :
* 그룹 1 금속 (알칼리 금속) 및 그룹 17 비금속 (Halogens) :염화나트륨 (NaCl), 칼륨 브로마이드 (KBR)
* 그룹 2 금속 (알칼리성 지구 금속) 및 그룹 16 비금속 (chalcogens) :산화 마그네슘 (MGO), 황화 칼슘 (CAS)
* 전이 금속 및 그룹 17 비금속 : 염화 구리 (Cucl2), 산화철 (Fe2O3)
중요한 참고 : 이러한 일반적인 추세에는 예외가 있습니다. 예를 들어, 일부 비금속은 다른 비금속 (예를 들어, 염화 암모늄 (NH4CL))과 이온 성 화합물을 형성 할 수있다.