더 자세한 설명은 다음과 같습니다.
* 황의 전자 구조 : 황 원자는 가장 바깥 쪽 껍질에 6 개의 전자가 있습니다. 안정적인 옥켓 구성을 달성하기 위해 2 개의 전자를 쉽게 얻습니다.
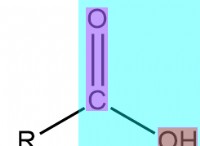
* 산소와의 반응 : 황이 산소에 노출되면 산소 원자와 결합하여 이산화황을 형성합니다 (SO2). 이 화학 반응은 매우 발열이므로 상당한 양의 열을 방출합니다.
* 연소 : 산소와의 반응 중에 방출 된 열은 황을 발화시켜 연소시킬 수 있습니다. 이 연소 과정은 연소로 알려져 있으며 황의 산소와의 빠른 반응으로 밝은 푸른 불꽃을 생성하고 이산화황 가스를 방출합니다.
중요한 참고 : 황의 가연성은 황 (분말, 덩어리 등), 온도 및 기타 물질의 존재를 포함한 여러 요인에 따라 다릅니다. 예를 들어, 황 먼지는 산소에 노출 된 표면적이 더 크기 때문에 고체 황보다 더 가연성 일 수 있습니다.
전반적으로, 황의 가연성은 산소와 쉽게 반응하는 경향이 있기 때문에 열과 빛의 형태로 에너지를 방출합니다.