용해도는 두 가지 주요 요인에 따라 다릅니다.
1. 극성 :
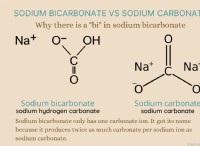
* 물은 극성 분자입니다 : 그것은 양의 끝 (수소)과 음의 끝 (산소)을 가지며 쌍극자 모멘트를 만듭니다.
* 알카 놀 및 알카노산에는 극 기능 그룹이 포함되어 있습니다.
* 알칸 놀스 : 히드 록실 그룹 (-OH)을 가지고 있으며, 이는 극성입니다.
* 알카노산 : 카르 복실 그룹 (-COOH)을 가지고 있으며, 이는 매우 극성입니다.
* "처럼 녹는 것처럼": 극성 분자는 다른 극성 분자에 용해되는 경향이 있습니다. 따라서, 알칸 놀 및 알카노산에 이들 극 기능 그룹의 존재는 물의 용해도에 기여한다.
2. 사슬 길이 (알칸올의 경우) :
* 단편 체인 알칸 놀스 : 더 짧은 탄소 사슬 (예를 들어, 메탄올, 에탄올, 프로 파놀)을 사용하면 극성 -OH 그룹이 우세하여 물에 용해됩니다.
* 장쇄 알칸올 : 탄소 사슬이 더 길어지면 비극성 탄화수소 부분이 더 중요해집니다. 비극성 부분은 분자가 물과 상호 작용하기가 더 어려워지고 용해성이 덜됩니다.
따라서 :
* 짧은 사슬 알칸올과 알카노산은 일반적으로 물에 용해됩니다. 극 기능 그룹은 탄화수소 사슬의 비극성 특성을 극복 할 수있을 정도로 강하다.
* 장쇄 알칸올은 물에 덜 용해됩니다. 비극성 탄화수소 부분이 지배적이며 -OH 그룹은 영향력이 적습니다.
주목하는 것이 중요합니다 : Solubility is not just about "yes" or "no." 정도의 문제입니다. 일부 알칸 놀 및 알카노산은 물에 부분적으로 용해 될 수 있으므로 제한된 정도로 용해 될 수 있습니다.
구체적인 예에 대해 자세히 설명하거나 다른 질문이 있으시면 알려주십시오!