이유는 다음과 같습니다.
* 옥트 규칙 : 비금속은 고귀한 가스와 같은 안정적인 전자 구성에 도달하기 위해 전자를 얻는 경향이 있습니다. 고귀한 가스에는 외부 껍질이 가득 차 있으므로 반응하지 않습니다.
* 원자가 전자 : 비금속에는 4-8 원자가 전자가있어 8에 도달하려면 4-0 전자를 얻어야합니다.
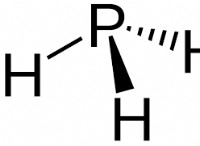
* 루이스 구조 : Lewis 구조는 도트를 사용하여 원자가 전자 및 선을 나타내며 공유 전자 쌍 (공유 결합)을 나타냅니다. 비금속 원자 주위의 점과 선은 최대 8 명을 추가해야합니다.
옥트 규칙에 대한 예외 :
* 수소 : 수소는 전체 외부 껍질 (헬륨)을 달성하기 위해 2 개의 전자 만 있으면됩니다.
* 붕소 : 붕소는 때때로 6 개의 전자만으로 안정적입니다.
* 더 큰 요소 : 3 및 그 이상의 일부 요소는 D 궤도의 가용성으로 인해 8 개 이상의 전자를 가질 수 있습니다.
예 :
* 산소 (O)는 8을 갖기 위해 2 개의 더 많은 전자가 필요합니다. 일반적으로 2 개의 결합을 형성합니다.
* 염소 (CL)는 8을 갖기 위해 1 개의 전자가 필요합니다. 일반적으로 하나의 결합을 형성합니다.
* 탄소 (c)는 8 개를 갖기 위해 4 개의 더 많은 전자가 필요합니다. 일반적으로 4 개의 결합을 형성합니다.
루이스 구조의 목표는 분자의 원자 주위의 전자 배열을 나타내어 결합과 안정성을 이해하는 데 도움이됩니다.