1. 화합물의 화학적 공식을 식별하십시오.
예를 들어, 물의 화학적 공식은 h₂o입니다.
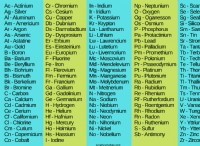
2. 화합물에서 각 원소의 원자 질량을 찾아보세요.
주기율표 에서이 값을 찾을 수 있습니다. 예를 들어, 수소 (H)의 원자 질량은 1.008 g/mol이고, 산소 (O)의 원자 질량은 15.9994 g/mol입니다.
3. 각 요소의 원자 질량을 화학식에서 첨자로 곱하십시오.
물의 경우 (h ofo) :
* 수소 (H) :1.008 g/mol * 2 =2.016 g/mol
* 산소 (O) :15.9994 g/mol * 1 =15.9994 g/mol
4. 화합물의 어금니 질량을 얻으려면 3 단계의 결과를 추가하십시오.
물 :2.016 g/mol + 15.9994 g/mol =18.0154 g/mol
따라서 물의 몰 질량 (H₂O)은 18.0154 g/mol입니다.
키 포인트 :
* 몰 질량은 두더지 당 그램 단위 (g/mol)로 표현됩니다.
* 화학적 공식의 첨자는 분자에서 각 요소의 원자 수를 나타냅니다.
*주기적인 테이블을 사용하여 원자 질량의 요소를 찾을 수 있습니다.
예 :
포도당의 몰 질량을 계산해 봅시다.
* 탄소 (C) :12.011 g/mol * 6 =72.066 g/mol
* 수소 (H) :1.008 g/mol * 12 =12.096 g/mol
* 산소 (O) :15.9994 g/mol * 6 =95.9964 g/mol
함께 추가 :72.066 g/mol + 12.096 g/mol + 95.9964 g/mol = 180.1584 g/mol
따라서, 포도당의 몰 질량은 180.1584 g/mol이다.