주요 차이 - Regiochemistry vs sterechemistry
Regiochemistry and sterechemistry는 화학의 두 가지 지점입니다. Regiochemistry는 Regioselective 반응의 화학입니다. 화학 반응이 어떻게 발생하는지 설명하는 용어입니다. regiosixectivity는 한 방향의 화학적 결합 제작 또는 다른 모든 방향에 걸쳐 파손되는 것을 선호합니다. 반면에 입체 화학은 유기 분자의 공간 배열에 대한 연구를 포함하는 화학 분야입니다. 입체 화학은 입체 이성질체의 배열을 설명합니다. Regiochemistry와 sterechochemistry의 주요 차이점은 Regiochemistry가 화학 반응의 최종 생성물의 원자 배열을 설명하는 반면, 입체 화학은 분자의 원자 배열과 그들의 조작을 설명한다는 것입니다. .
주요 영역을 다루었습니다
1. regiochemistry
- 정의, Markovnikov의 규칙 및 Anti Markovnikov의 규칙
2. 입체 화학이란 무엇입니까
- 정의, 입체 이성질체, 기하학적 이성질체, 광학 이성질체, 키랄성
3. Regiochemistry와 sterechemistry의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :CIS 이성질체, 기하학적 이성질체, 이성질체, Regiocheomistry, Regiosexectivity, sterechemistry, stereoisomer, 트랜스 이성질체

regiochemistry
regiochemistry는 화학 반응의 regiosixectivity를 설명하는 화학 분야입니다. regiosixectivity는 반응 생성물의 배열에서 다른 모든 가능한 방향보다 하나의 방향을 선호합니다.
regiochemistry는 어떤 제품이 주요 제품인지, 어떤 제품이 여러 제품을 제공하는 화학 반응에서 작은 제품인지를 나타냅니다. 이것은 시약 분자가 첨가 될 표적 분자의 가능한 위치에 의존한다. 예를 들어, 치환 된 벤젠 고리에서 시약 분자는 세 가지 가능한 위치 중 하나 인 ortho 에 부착 될 수 있습니다. , para 및 메타 벤젠 고리에 이미 존재하는 치환기에 따라 위치.
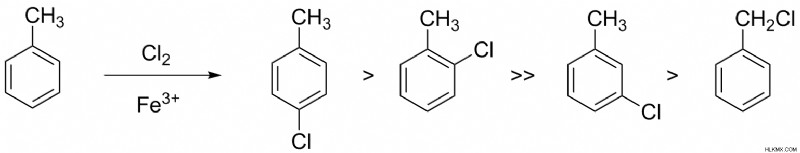
그림 1 :톨루엔 염소화는 regioselective 입니다
위의 반응은 톨루엔의 염소화를 보여줍니다. 염소 원자가 톨루엔 분자에 부착 될 수있는 몇 가지 가능한 위치가 있습니다. 그러나 파라 대체는 무엇보다도 가장 안정적입니다. 따라서이 반응에 의해 주어진 주요 제품입니다.
특정 화학 반응의 주요 제품이 무엇인지 결정하기 위해 몇 가지 규칙이 도입되었습니다. 첫 번째 규칙은 Markovnikov의 규칙입니다. Markovnikov Rule에 따르면, 양성자는 알켄 또는 알킨의 반응에서 그것에 부착 된 수소 원자가 가장 많은 탄소 원자에 첨가된다. 이 규칙은 특정 화학 반응의 최종 생성물을 예측하는 데 도움이됩니다.
그러나, 나중에 도입 된 Anti Markovnikov 규칙에 따르면, 나중에 도입 된 알켄 또는 알킨스의 반응에서, 양성자는 그에 부착 된 수소 원자가 가장 적은 탄소 원자에 첨가된다. 이 반응으로부터 얻은 최종 생성물을 항 마르코프 니코프 제품이라고한다. 이 메커니즘은 탄수화물 중간체의 형성을 포함하지 않습니다. 화학 반응은 반응 혼합물에 HOOH와 같은 과산화물을 첨가함으로써 항 마르코프 니코프 생성물을 제공하는 반응으로 만들어 질 수있다.
.Regiochemistry에 관한 다른 규칙은 친핵체의 추가 반응에 대한 fürst-plattner 규칙, 고리-폐쇄 반응의 regiosexectivity 등을위한 Baldwin의 규칙을 포함합니다.
.입체 화학이란 무엇입니까
입체 화학은 유기 분자의 공간 배열과 그들의 조작에 대한 연구를 포함하는 화학의 분야입니다. 입체 이성질체에 대한 연구가 포함됩니다. 입체 이성질체는 동일한 분자 공식 및 원자 배열을 갖는 분자이지만 다른 공간 배열이다. 입체 이성질체의 두 주요 그룹은 다음과 같습니다.
- 기하학적 이성질체
- 광학 이성질체
기하학적 이성질체는 cis-trans 로도 알려져 있습니다 이성질체. 이 이소머는 항상 쌍으로 발생합니다. 2 개의 이성질체는 시스-이성질체 및 트랜스 이성질체이다. 이 이성질체는 이중 결합을 갖는 분자에서 발생합니다. 비닐 탄소 원자에 기능적 그룹의 부착은 이들 두 이성질체의 차이이다. (비닐 탄소는 다른 탄소 원자와 이중 결합을 갖는 탄소 원자입니다.)
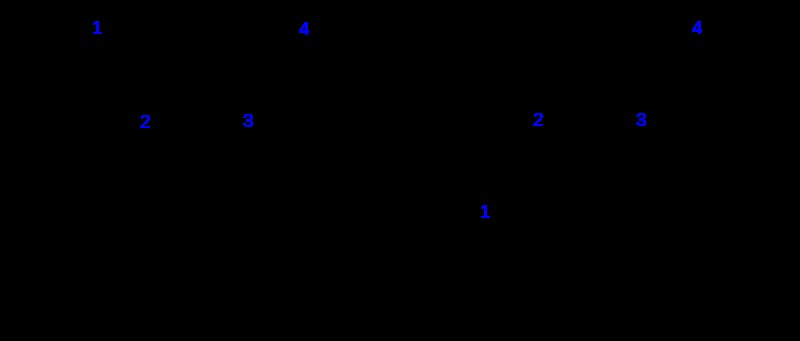
그림 2 :기하학적 이성질체
또한 입체 화학은 키랄성의 개념을 설명합니다. 키랄성은 거울 이미지가 분자와 감독 할 수 없다고 말하는 분자의 특성입니다. 키랄 탄소는 비대칭 탄소입니다. 탄소 원자는 최대 4 개의 결합을 가질 수 있습니다. 키랄 탄소는 4 개의 다른 그룹에 결합되며 비대칭입니다. 탄소 원자는 키랄 탄소가 되려면 항상 SP 혼성화되어야합니다. 키랄 분자는 일반적으로 적어도 하나의 키랄 탄소를 함유합니다. SP 또는 SP2 혼성 탄소 원자는 π- 결합의 존재로 인해 주변에 4 개의 다른 그룹을 가질 수 없기 때문에 키랄이 될 수 없습니다. 광학 이성질체는 키랄 탄소가있는 분자에서 발생합니다. 이 키랄 탄소는 입체 이성질체의 발생을 유발합니다. 이는 해당 분자의 감독 할 수없는 미러 이미지입니다.
Regiochemistry와 입체 화학의 차이
정의
regiochemistry : Regiochemistry는 화학 반응의 regioselectivity를 설명하는 화학 분야입니다.
입체 화학 : 입체 화학은 유기 분자의 공간적 배열과 그들의 조작에 대한 연구를 포함하는 화학 분야입니다.
초점
regiochemistry : Regiochemistry는 특정 화학 반응의 최종 생성물을 결정하는 데 사용되는 규칙을 설명합니다.
입체 화학 : 입체 화학은 다른 입체 이성질체의 원자 배열을 설명합니다.
사양
regiochemistry : Regiochemistr에는 Markovnikov Rule, Anti Markovnikov Rule, Fürst-Plattner Rule, Baldwin 's Rule 등과 같은 중요한 규칙이 포함됩니다.
입체 화학 : 입체 화학은 기하학적 이성질체, 광학 이성질체 및 분자의 키랄성을 포함합니다.
결론
Regiochemistry and sterechemistry는 화학의 두 가지 중요한 하위 범주입니다. Regiochemistry와 sterechochemistry의 주요 차이점은 Regiochemistry가 화학 반응의 최종 생성물의 원자 배열을 설명하는 반면, 입체 화학은 분자의 원자 배열과 그들의 조작을 설명한다는 것입니다.
참조 :
1.“Regiosexectivity.” Wikipedia, Wikimedia Foundation, 2018 년 1 월 13 일, 여기에서 구입할 수 있습니다.
이미지 제공 :
1. Mfomich에 의한“Regioselectivity toluene 염소화” - Commons Wikimedia
2를 통한 자신의 작업 (CC0). Jaga의 "Cis-Trans 예"-Commons Wikimedia를 통해 Bkchem 및 Inkscape (CC By-SA 3.0)를 사용하여 자체 제작했습니다.