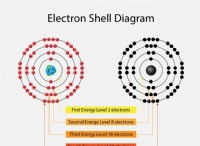
* 안정성 : 원자는 안정적인 전자 구성, 일반적으로 전자의 전체 외부 쉘을 사용하여 노력합니다. 이것은 가장 활발한 상태입니다.
* 정전기력 : 반대로 하전 된 입자 (핵 및 전자의 양성자와 같은) 사이의 인력은 매우 강합니다.
이온이 형성되는 방법
* 양이온 형성 : 원자가 전자를 잃으면 전자보다 양성자 (양성)가 많기 때문에 긍정적으로 하전됩니다 (음수). 이것을 양이온이라고합니다 .
* 음이온 형성 : 원자가 전자를 얻을 때, 이제 양성자 (양성)보다 전자 (음수)가 많기 때문에 음으로 하전됩니다. 이를 음이온이라고합니다 .
예 :
* 나트륨 (NA)은 Na+ (나트륨 이온)가되기 위해 하나의 전자를 잃는다 . 이는 전자를 잃어 버림으로써 나트륨은 외부 쉘이 완전한 네온 (NE)과 같은 안정적인 전자 구성을 달성하기 때문입니다.
* 염소 (Cl)는 하나의 전자를 얻기 위해 Cl- (클로라이드 이온)를 얻습니다. . 전자를 얻음으로써 염소는 아르곤 (AR)과 같은 안정적인 전자 구성을 달성합니다.
키 포인트 :
* 이온 형성은 화학의 기본 과정입니다.
* 이온은 화학 반응, 특히 용액에 필수적입니다.
* 이온의 형성은 안정성에 대한 욕구와 반대 전하 사이의 강한 정전기 인력에 의해 구동된다.