이유는 다음과 같습니다.
* 끓는점 액체가 가스로 변하는 온도입니다.
* 분자 력 분자들 사이의 매력입니다. 더 강한 분자간 힘은 더 많은 에너지가 파손되어 더 높은 끓는점을 초래합니다.
예 :
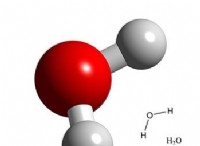
* 물 (H2O)은 100 ° C (212 ° F)에서 끓습니다. 수소 결합은 강한 분자간 힘입니다.
* 에탄올 (C2H5OH)은 78.4 ° C (173 ° F)에서 끓습니다. 물보다 수소 결합이 약합니다.
* 아세톤 (CH3Coch3)은 56 ℃ (133 ° F)에서 끓는다. 쌍극자 쌍극자 힘이 약합니다.
* 헬륨 (HE)은 -268.93 ° C (-452.07 ° F)에서 끓습니다. 런던 분산 세력이 매우 약합니다.
결론적으로 물질의 끓는점은 분자간 힘의 강도에 의해 결정되며, 다른 물질은 분자간 힘을 갖는다.