염의 화학적 특성 :
염은 산의 염기와의 반응에 의해 형성된 이온 성 화합물이다. 그것들은 다음을 포함하여 다양한 화학적 특성을 특징으로합니다.
1. 전해질 : 염은 강한 전해질이므로 이온을 형성하여 전기를 전도하는 용액에 완전히 분리됩니다. 이 특성은 배터리 및 전기 도금을 포함한 다양한 응용 프로그램에 필수적입니다.
2. 산 및 염기와의 반응성 :
* 산과의 반응 : 염은 더 강한 산과 반응하여 새로운 염과 원래 염의 상응하는 산을 형성합니다. 예를 들어, 염화나트륨 (NaCl)은 질산 나트륨 (NANO3) 및 염산 (HCL)을 형성하기 위해 질산 (HNO3)과 반응합니다.
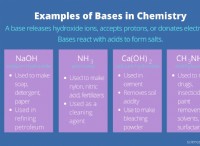
* 염기와의 반응 : 염은 더 강한 염기와 반응하여 새로운 염과 원래 소금의 상응하는 기초를 형성 할 수 있습니다. 예를 들어, 염화 암모늄 (NH4CL)은 수산화 나트륨 (NaOH)과 반응하여 염화나트륨 (NaCl) 및 암모니아 (NH3)를 형성합니다.
3. 용해도 :
* 수용성 : 물 내 염의 용해도는 존재하는 양이온 및 음이온에 따라 크게 다릅니다. 염화나트륨 (NaCl)과 같은 일부 염은 매우 용해성이지만, 바륨 설페이트 (BASO4)와 같은 다른 염은 실질적으로 불용성입니다.
* 다른 용매에서의 용해도 : 염은 또한 화학 구조와 용매의 특성에 따라 물 외에 다른 용매에 용해 될 수 있습니다.
4. 열 안정성 :
* 분해 : 일부 염은 가열 될 때 분해되어 산화물, 원소 또는 기타 염을 형성합니다. 예를 들어, 탄산 칼슘 (CACO3)은 가열시 분해되어 산화 칼슘 (CAO) 및 이산화탄소 (CO2)를 형성합니다.
* 용융점 : 염은 일반적으로 이온 사이의 강한 정전기 상호 작용으로 인해 높은 용융점을 갖는다.
5. pH :
* 중성 소금 : 강산 및 강한 염기로부터 형성된 염은 pH 7의 중성이다.
* 산성 소금 : 강산 및 약한 염기로부터 형성된 염은 산성이며, pH는 7 미만이다.
* 기본 소금 : 약산 및 강한 염기로부터 형성된 염은 기본이며, pH는 7보다 큰 기본이다.
6. 산화 환원 반응 :
* 산화 감소 : 일부 염은 산화 환원 반응에서 산화 또는 환원제 역할을 할 수 있습니다. 예를 들어, 칼륨 과망간산염 (KMNO4)은 다양한 화학 반응에 사용되는 강력한 산화제입니다.
7. 기타 화학 반응 :
* 강수 반응 : 염은 불용성 침전물을 형성하기 위해 반응 할 수 있습니다. 예를 들어, 질산은 (Agno3)은 염화나트륨 (NaCl)과 반응하여 염화은 침전물 (AGCL)을 형성합니다.
* 복잡한 형성 : 일부 염은 다른 종과 복잡한 이온을 형성 할 수 있습니다. 예를 들어, 황산 구리 (CUSO4)는 암모니아 (NH3)와 반응하여 깊은 푸른 복합체 이온, 테트라 암민 콥 (II) 이온 ([Cu (NH3) 4] 2+)를 형성한다.
응용 프로그램 :
소금은 다음을 포함하여 다양한 산업에서 광범위한 응용 프로그램을 가지고 있습니다.
* 식품 산업 : 염은 향미 인한자, 방부제 및 발효 과정을 제어하는 데 사용됩니다.
* 농업 : 염은 식물에 필수 영양소를 공급하기 위해 비료로 사용됩니다.
* 제약 : 소금은 다양한 약물과 제약 제품을 생산하는 데 사용됩니다.
* 화학 산업 : 염은 다양한 화학 공정에서 시약, 촉매 및 중간체로 사용됩니다.
* 기타 응용 프로그램 : 소금은 건축, 섬유 및 기타 여러 산업에도 사용됩니다.
염의 화학적 특성을 이해하는 것은 다양한 응용 분야에서 안전하고 효율적으로 사용하는 데 중요합니다. 그들의 다양한 속성과 반응성은 많은 산업 과정과 일상 생활에서 필수 구성 요소를 만듭니다.