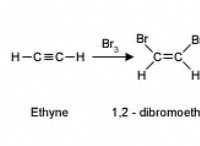
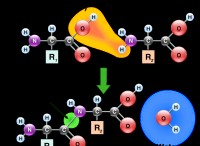
* 행동 메커니즘 : 촉매는 활성화 에너지가 낮은 대안적인 반응 경로를 제공함으로써 작용한다. 그들은 반응물과 상호 작용하고 일시적인 중간체를 형성 한 다음 추가 반응에 참여하기 위해 풀려납니다.
* 효율성 : 단일 촉매 분자는 수많은 반응을 촉진 할 수 있습니다. 그들은 그 과정에서 소비되지 않으므로 반복적으로 재사용 할 수 있습니다.
* 최적화 : 필요한 촉매의 양은 특정 반응 및 원하는 속도에 따라 달라질 수 있습니다. 너무 많은 촉매는 원치 않는 부작용이나 합병증을 유발할 수 있습니다.
예 :
* 효소 : 이들 생물학적 촉매는 엄청나게 효율적이다. 그것들은 세포 내에 미세한 양으로 존재하지만 생화학 적 반응 속도를 크게 높일 수 있습니다.
* 산업 공정 : 많은 산업 공정에서 촉매는 소량으로 사용하여 효율성을 극대화하고 비용을 최소화합니다. 예를 들어, 암모니아 합성을위한 Haber-Bosch 공정은 철 촉매를 사용합니다.
예외 :
소량의 양은 일반적으로 충분하지만, 더 높은 촉매 로딩이 필요한 경우가 있습니다.
* 느린 반응 : 매우 느린 속도를 갖는 반응의 경우, 원하는 반응 속도를 달성하기 위해 더 높은 촉매 농도가 필요할 수있다.
* 이종 촉매 : 경우에 따라, 특히 고체 촉매의 경우, 반응물과의 최적의 상호 작용을 위해서는 더 큰 표면적이 필요하다. 이것은 더 높은 촉매 로딩이 필요할 수 있습니다.
요약 : 촉매는 일반적으로 매우 효율적이고 반응에서 소비되지 않기 때문에 소량으로 사용됩니다. 그러나 필요한 정확한 양은 특정 반응 및 원하는 결과에 따라 달라질 수 있습니다.