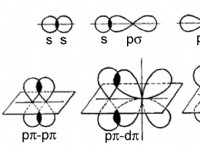
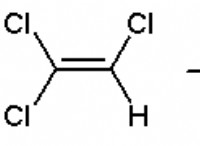
* 혼성화 : 분자의 각각의 탄소 원자는 전자 밀도의 3 가지 영역, 즉 2 개의 단일 결합과 1 개의 이중 결합을 갖는다. 이로 인해 SP² 하이브리드 화가 발생하여 각 탄소 주위에 삼각형 평면 형상이 생깁니다.
* 결합 각도 : 분자의 결합 각도는 대략 120도이며, 삼각 평면 형상과 일치합니다.
이를 시각화하는 단순화 된 방법은 다음과 같습니다.
1. 중앙 탄소 : 중간의 탄소 원자는 다른 두 개의 탄소 원자에 연결되어 있으며 그 중 하나와 이중 결합을 갖습니다.
2. 삼각 평면 : 이 중심 탄소는 평평하고 삼각형 모양을 형성하며, 3 개의 부착 된 원자 (2 개의 탄소 및 1 개의 수소)가 모서리에 형성됩니다.
3. 전체 모양 : 전체 분자는 이중 결합으로 인해 약간의 "지그재그"가있는 평평하고 길쭉한 모양으로 간주 될 수 있습니다.
더 자세한 설명을 원하거나 다른 질문이 있으시면 알려주세요!