주요 차이 - 시그마 대 PI 본드
Sigma와 Pi 결합은 3 ~ 2 개의 원자를 갖는 공유 결합 및 분자의 일부 특징을 설명하는 데 사용됩니다. 이 본드는 불완전한 s 의 겹쳐서 형성됩니다. 및 p 결합에 참여하는 두 원자의 궤도. 따라서이 모델은 종종 오버랩 모델이라고합니다. 이 모델은 주로 작은 원자의 결합 형성을 설명하기 위해 적용되며 더 큰 분자의 결합을 설명하는 데 적용 할 수 없습니다. 시그마 본드와 PI 본드의 주요 차이점은 그들의 형성이다. 두 궤도 형태의 축 방향 겹치는 시그마 본드 while 두 궤도의 측면 중첩 형태 pi bond .
이 기사는
를 탐구합니다 1. 시그마 본드
- 정의, 특성, 속성
2. PI 본드
- 정의, 특성, 속성
3. Sigma와 Pi Bond의 차이점은 무엇입니까
시그마 본드
두 원자의 원자 궤도의 동축 또는 선형 중첩은 시그마 결합을 형성합니다. 단일, 이중 및 삼중 본드에서 발견되는 주요 결합입니다. 그러나 두 원자 사이에는 하나의 시그마 결합 만있을 수 있습니다. 시그마 본드는 시그마 본드가 원자 궤도의 최대 겹치기 때문에 PI 결합보다 강하다. 본드 축을 따라있는 단일 전자 구름이 포함되어 있습니다. 시그마 본드는 공유 결합의 형성 동안 형성되는 최초의 결합이다. PI 결합과 달리, 혼성화 된 및 가이 브리지 화 된 궤도는 시그마 결합을 형성합니다.
pi bond
pi bond는 원자 궤도의 측면 또는 측면 또는 평행 중첩으로 형성됩니다. 이러한 채권은 겹치는 최소 범위로 인해 시그마 채권보다 약합니다. 또한, PI 결합은 시그마 결합의 형성 후에 형성된다. 따라서 이러한 유대는 항상 시그마 본드로 존재합니다. PI 결합은 수익 조절되지 않은 P-P 원자 궤도의 겹쳐서 형성된다. 시그마 결합과 달리, PI 결합은 분자의 모양에 영향을 미치지 않습니다. 단일 채권은 시그마 본드입니다. 그러나 이중 및 삼중 채권에는 시그마 본드와 함께 각각 1 및 2 개의 PI 결합이 있습니다.
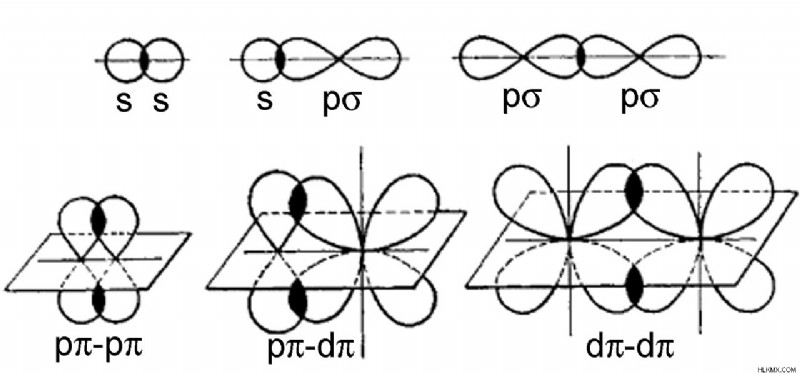
그림 01 :Sigma Bond and Pi Bond
Sigma와 Pi Bond
의 차이채권 형성
시그마 본드 : 시그마 본드는 원자의 반으로 채워진 원자 궤도의 축 방향 중첩에 의해 형성됩니다. .
Pi Bond : PI 결합은 원자의 반 채로 된 원자 궤도의 측면 중첩에 의해 형성됩니다.
겹치는 궤도
Sigma Bond : 시그마 본드에서 겹치는 궤도는 2 개의 하이브리드 궤도 또는 하나의 하이브리드 및 1 개의 순수한 궤도 또는 2 개의 순수한 궤도
가 될 수 있습니다.pi bond : PI 결합에서, 겹치는 궤도는 항상 두 개의 순수 (즉, 비료화 된) 궤도입니다.
존재
시그마 본드 : 시그마 본드는 독립적으로 존재합니다.
Pi Bond : Pi-bond는 항상 Sigma Bond와 함께 존재합니다.
2 개의 탄소 원자의 회전
시그마 본드 : 시그마 본드는 자유 회전을 허용합니다.
Pi Bond : Pi Bond는 자유 회전을 제한합니다.
결합 강도
시그마 본드 : 시그마 본드는 PI 결합보다 강합니다.
Pi Bond : PI 본드는 시그마 본즈보다 덜 강합니다.
본드 형성 순서
시그마 본드 : 원자가 더 가까워지면 시그마 결합이 먼저 형성됩니다.
Pi Bond : PI 결합의 형성은 시그마 본즈의 형성에 의해 선행됩니다.
채권 수
시그마 본드 : 두 원자 사이에는 하나의 시그마 결합이 있습니다.
Pi Bond : 두 원자 사이에는 두 개의 PI 결합이있을 수 있습니다.
다 원자 분자에서 형상의 제어
시그마 본드 : 시그마 결합만이 다 원자 분자에서 기하학의 제어에 관여합니다.
Pi Bond : PI 결합은 다 원자 분자에서 기하학의 제어에 관여하지 않습니다.
이중 채권에서 채권 수
시그마 본드 : 이중 채권에는 하나의 시그마 본드가 있습니다.
Pi Bond : 이중 채권에는 하나의 PI 본드 만 있습니다.
트리플 본드에서 채권 수
시그마 본드 : 트리플 본드에는 시그마 본드가 하나 있습니다.
Pi Bond : 트리플 본드에는 두 개의 PI 결합이 있습니다.
전하 대칭
시그마 본드 : 시그마 본드는 본드 축 주위에 원통형 전하 대칭을 가지고 있습니다.
Pi Bond : Pi Bond. 대칭이 없습니다.
반응성
시그마 본드 : 시그마 본드는 더 반응성입니다.
Pi Bond : PI 결합은 덜 반응성입니다.
모양 결정
시그마 본드 : 분자의 모양은 시그마 본드에 의해 결정됩니다.
Pi Bond : 분자의 모양은 pi 결합에 의해 결정되지 않습니다.
요약
Sigma와 Pi는 두 개의 원자 궤도로 인해 형성된 두 가지 유형의 결합입니다. 두 원자의 축 중첩은 시그마 결합을 형성하는 반면, 두 원자 궤도의 측면 중첩은 시그마 결합을 형성합니다. 이것이 Sigma와 Pi Bond의 주요 차이점입니다. 시그마 본드는 항상 먼저 형성되며 Pi Bond보다 강합니다. 단일 채권은 항상 시그마 채권이며, 이중 채권과 트리플 본드는 시그마 본드와 함께 각각 1 및 2 개의 PI 결합을 갖는다.
.
참고 문헌
1. Mohapatra, R. K. (2014). 디플로마 공학 화학 . Phi Learning Pvt. Ltd ..
2. Srivastava, A. K. (2002). 유기 화학은 간단하게 만들어졌다 . New Age International.
3. Jespersen, N.D., &Hyslop, A. (2014). 화학 :물질의 분자 특성 :물질의 분자 특성 와일리 글로벌 교육.